下列热化学方程式中,ΔH能正确表示物质的燃烧热的是
| A.CO(g)+1/2O2(g)====CO2(g) ΔH=-283.0 kJ·mol-1 |
| B.C(s)+1/2O2(g)====CO(g) ΔH=-110.5 kJ·mol-1 |
| C.H2(g)+1/2O2(g)====H2O(g) ΔH=-241.8 kJ·mol-1 |
| D.2C8H18(l)+25O2(g)====16CO2(g)+18 H2O(l) ΔH=-11036 kJ·mol-1 |
下列物质的水溶液中,pH值 大于7的是
大于7的是
| A.Na2CO3 | B.NH4NO3 | C.Na2SO4 | D.KNO3 |
一定量的某有机物完全燃烧后,将燃烧产物通过足量的澄清石灰水,经过滤可得沉淀10g,但称量滤液时,其质量比反应前减少2.9g,则此有机物可能是
| A.乙烯 | B.丙三醇 | C.乙醇 | D.乙酸 |
在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,则这个碳原子称为“手性碳原子”凡是只有一个手性碳原子物质一定具有光学活性,物质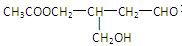 有光学活性,发生下列反应后无光学活性的是
有光学活性,发生下列反应后无光学活性的是
| A.与新制的Cu(OH)2作用 | B.与甲酸发生 酯化反应 酯化反应 |
| C.与NaOH水溶液共热 | D.在催化剂存在下与H2加成 |
下列装置或操作不能达到的实验目的是
对如图结构的有机物的下列叙述中,不正
 确的是
确的是
| A.常温下,能与Na2CO3溶液反应放出CO2气体 |
| B.能发生碱性水解,lmol该有机物完成反应最多需消耗8molNaOH |
| C.与稀硫酸共热,生成两种有机物 |
| D.该有机物的化学式是C14H10O9 |