已知:2Zn(s) + O2(g)= 2ZnO(s) △H1= -701.0kJ·mol-1,2Hg(l)+ O2(g)= 2HgO(s) △H2= -181.6kJ·mol-1,则反应Zn(s) + HgO(s)= ZnO(s) + Hg(l)的△H为:
| A.+519.4 kJ·mol-1 | B.+259.7 kJ·mol-1 |
| C.-259.7 kJ·mol-1 | D.-519.4 kJ·mol-1 |
在盛有饱和碳酸钠溶液的烧杯中插入惰性电极,保持温度不变,通电一段时间后
| A.溶液的pH增大 | B.Na+ 和CO32-的浓度减小 |
| C.溶液的浓度增大 | D.溶液的浓度不变,有晶体析出 |
以Mg片和Al片为电极,并用导线连接,同时插入NaOH溶液中,下列说法正确的是
A.Mg片作负极,电极反应:Mg-2e-  Mg2+ Mg2+ |
B.Al片作负极,电极反应:Al+4OH- -3e-  AlO2- +2H2 O AlO2- +2H2 O |
| C.电子从Mg电极沿导线流向Al电极 |
| D.Al片上有气泡产生 |
2A(g)+B(g)  3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是
3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是
A.v(A) = 0.7mol·L-1·min-1B.v(B) = 0.3mol·L-1·min-1
C.v(C) = 0.9mol·L-1·min-1 D.v(D) = 1.1mol·L-1·min-1
根据热化学方程式(在101 kPa时):S(s)+O2(g)=SO2(g) ΔH=-297.2kJ/mol
分析下列说法中不正确的是
| A.S的燃烧热为 297.2 kJ/mol |
| B.S(g)+O2(g)=SO2(g)放出的热量大于297.2 kJ |
| C.S(g)+O2(g)=SO2(g)放出的热量小于297.2 kJ |
| D.形成1 mol SO 2 中的化学键所释放的总能量大于断裂1 mol S(s)和1 mol O2(g)中的化学键所吸收的总能量 |
关于中和热测定实验的下列说法不正确的是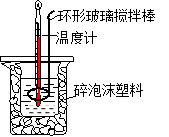
| A.烧杯间填满碎泡沫塑料是减少实验过程中的热量损失 |
| B.使用环形玻璃棒既可以搅拌又避免损坏温度计 |
| C.向盛装酸的烧杯中加碱时要小心缓慢的分几次加入 |
| D.测了酸后的温度计要用水清洗后再测碱的温度 |