在一定体积的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:aA(g)+bB(g) xC(g),符合下图所示的关系(C%表示平衡混合气中产物C的百分含量,T表示温度,P表示压强)。在图中Y轴是指
xC(g),符合下图所示的关系(C%表示平衡混合气中产物C的百分含量,T表示温度,P表示压强)。在图中Y轴是指
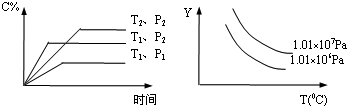
①反应物A的转化率,②平衡混合气中物质B的百分含量,
③平衡混合气的密度,④平衡混合气的平均摩尔质量
A.①③ B.②③ C.③④ D.①④
在下图装置中,烧瓶中充满干燥 气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中
气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中 的液体c呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是
的液体c呈喷泉状喷出,最终几乎充满烧瓶.则a和b分别是
| a(干燥气体) |
b(液体) |
|
| A |
NO2 |
水 |
| B |
CO2 |
4mol/LNaOH溶液 |
| C |
Cl2 |
饱和NaCl水溶液 |
| D |
NH3 |
1mol/L盐酸 |
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等因素有关。下列各组物质中由于浓度不同而能发生不同氧化还原反应的是
| A.Cu与HNO3溶液 | B.Cu与FeCl3溶液 |
| C.Zn与H2SO4溶液 | D.Fe与HCl溶液 |
硫代硫酸钠可作为脱氯剂 ,已知25.0mL0.100mol/LNa2S2O3溶液恰好把224mL(标准状况下)Cl2完全转化为Cl-离子,则S2O32—将转化成
,已知25.0mL0.100mol/LNa2S2O3溶液恰好把224mL(标准状况下)Cl2完全转化为Cl-离子,则S2O32—将转化成
| A.S2— | B.S | C.SO32— | D.SO42— |
某金属单质跟一定浓度的硝酸反应,假定只产生单一的还原产物.当参加反应的单质与被还原硝酸的物质的量之比为2:1时,还原产物是
| A.NO2 | B.NO | C.N2O | D.NH4NO3 |
38.4毫克铜跟适量的浓硝酸反应,铜全部作用后共收集到气体22.4毫升(标准状况),反应消耗的HNO3的物质的量可能是
| A.1.0×10-3摩尔 | B.1.6×10-3摩尔 |
| C.2.2×10-3摩尔 | D.2.0×10-3摩尔 |