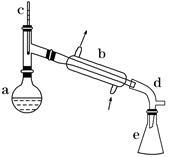
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
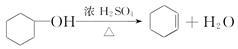
可能用到的有关数据如下:
| |
相对分子质量 |
密度/(g·cm-3) |
沸点/℃ |
溶解性 |
| 环己醇 |
100 |
0.961 8 |
161 |
微溶于水 |
| 环己烯 |
82 |
0.810 2 |
83 |
难溶于水 |
合成反应:
在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸。b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是_______________。
(2)加入碎瓷片的作用是________________;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是________(填正确答案标号)。
A.立即补加 B.冷却后补加
C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为______________。
(4)分液漏斗在使用前须清洗干净并________;在本实验分离过程中,产物应该从分液漏斗的________(填“上口倒出”或“下口放出”)。
(5)分离提纯过程中加入无水氯化钙的目的是_______________。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有________(填正确答案标号)。
A.圆底烧瓶
B.温度计
C.吸滤瓶
D.球形冷凝管
E.接收器
(7)本实验所得到的环己烯产率是____________(填正确答案标号)。
A.41% B.50% C.61% D.70%
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
已知:①海水中溴元素(以Br-表示)的浓度0.068g/L;
②Br2的沸点为59 ℃,微溶于水,有毒性和强腐蚀性。
(1)请写出一种海水淡化的方法:_____________。
(2)海水中溴离子的物质的量浓度为_____________ 。
(3)步骤Ⅰ中已获得低溶度的含Br2溶液,步骤Ⅱ中又将Br2还原为Br-,步骤Ⅲ又得到Br2,其目的为________________。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 。
(5)工业溴提纯可用蒸馏法,蒸馏时加热方法最好采用 ,蒸馏装置中仪器连接均不能用橡胶塞和橡胶管,其原因是_________________________________。
在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘:
试完成下列问题:
(1)乙、丁中溶质的化学式:乙____________;丁____________。
(2)第④步操作中用稀H2SO4浸洗的目的是____________(填写字母编号)。
a.除去未反应的 b.除去未反应的I-
b.除去未反应的I-
c.除去未反应的Fe d.除去碱性物质
(3)第⑦步操作可供提纯I2的一种方法是____________(不要求写具体步骤)。
(4)实验室检验I2的方法是________________________。
(5)甲物质见光易变黑,其原因是______________________________(用化学方程式表示)。
铁砂的主要成分是微粒状的磁性氧化铁、石英、石灰石等混合物。某化学兴趣小组从铁砂中分离出磁性氧化铁,并进行铝热反应实验。
(1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是______________,
现象很壮观,取少许反应生成的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色。出现这种结果的原因,除了可能混有没反应的磁性氧化铁外,还有一个原因是 。
(2)设计一个简单的实验方案,证明上述所得的“铁块”中含有金属铝。该实验所用试剂是_________,反应的离子方程式为_________________________________。
(3)请写出此铝热反应的化学方程式: 。
每摩铝参与反应,转移的电子数为 。
(4)生成除磁性氧化铁可做铝热反应实验外,下列哪些试剂也可以________。
| A.CuO | B.Na2O2 | C.MnO2 | D.MgO |
下图为硬脂酸甘油酯在碱性条件下水解的装置图,进行皂化反应时的步骤如下:
(1)在圆底烧瓶中装入7~8 g硬脂酸甘油酯,然后加入2~3 g的氢氧化钠、5 mL水和10 mL酒精;加入酒精的作用为_______________________________。
(2)向所得混合物中加入_______,静置一段时间,溶液分为上下两层,肥皂在___层。
(3)图中长玻璃管的作用是________________________________________________。
(4)写出该反应的化学方程式______________________________________________。
某化学课外活动小组研究乙醇氧化的实验并验证其产物,并从“乙醇催化氧化实验”得到一些认识有关催化剂的催化机理等问题。
(1)甲同学其实验操作为:预先使棉花团浸透乙醇,并按下图搭好实验装置;在铜丝的中间部分加热,片刻后开始有节奏(间歇性)地鼓入空气,即可观察到明显的实验现象。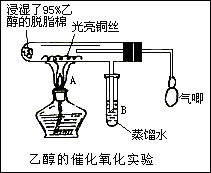
请回答以下问题:
①被加热的铜丝处发生的反应的化学方程式为________。
②从A管中可观察到 实验现象。
(2)乙同学研究乙醇氧化的实验并验证其产物,组合一套实验装置(图中的夹持仪器均未画出,“△”表示酒精灯热源),仪器中盛放的试剂为:a-无水乙醇(沸点:78 ℃);b-铜丝;c-无水硫酸铜;d-新制氢氧化铜悬浊液。
①若要保证此实验有较高的效率,还需补充的仪器有___________。理由____________。
②实验中能验证乙醇氧化产物的实验现象是__________________________。
③装置中,若撤去高锰酸钾加热部分并用夹子夹K,其它操作不变,则无水硫酸铜无明显变化,其余现象与②相同,推断燃烧管中主要反应的化学方程式___________________。