如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同。打开活塞,使NO与O2充分反应。(不考虑NO2与N2O4的转化)
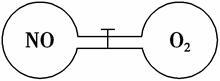
(1)开始时左右两室分子数 (填“相同”或“不相同”)。
(2)反应前后NO室压强 (填“增大”或“减小”) 。
(3)最终容器内密度与原来 (填“相同”或“不相同”)。
(4)最终容器内 (填“有”或“无”)O2存在。
A、B、C、D、E均为短周期主族元素,且原子序数依次递增。A、E同主族,B、D同周期且B和D最外层电子数之和为10;D为自然界含量最多的元素;A与D可形成A2D、A2D2共价化合物。请回答:
(1)C的气态氢化物的电子式为______,其水溶液显性。
(2)B、C、D气态氢化物稳定性由强到弱的顺序是________________(用化学式表示)。
(3)与E同周期的元素中,金属性最弱的金属元素名称是,原子结构示意图为:,其最高价氧化物对应的水化物与E的最高价氧化物对应的水化物的溶液反应的离子方程式为。
(4)E、C两元素的最高价氧化物对应水化物的稀溶液各0.1mol,恰好完全反应,放出5.73kJ的热量,写出此反应的热化学方程式:。
航天技术使用氢氧电池具有高能、轻便,不污染优点,氢氧燃料电池有酸式和碱式两种,它们放电时的电池总反应式均可表示为:2H2+O2 = 2H2O ,酸式氢燃料电池的电解质是酸、其负极反应为:2H2-4e-= 4H+,则正极反应为 ;碱式氢氧燃料电池的电解质是碱,其正极反应表示为:O2+2H2O+4e-= 4OH-,则负极反应为: 。
在一定条件下,将3molA 和1mol B 两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+ 2D(g)。2min末该反应达到平衡,生成0.8mol D ,并测得C的浓度为0.2mol·L-1。请填空:
xC(g)+ 2D(g)。2min末该反应达到平衡,生成0.8mol D ,并测得C的浓度为0.2mol·L-1。请填空:
(1)x=__________
(2)正反应是放热反应,则升高温度,正反应速率,逆反应速率。(填升高、降低或不变)
(3)B的转化率为_________。
(4)能判断该反应达到平衡状态的依据是________(填字母)
| A.混合气体的密度不变 |
| B.容器中的压强不再变化 |
| C.生成D的反应速率是生成B的反应速率的2倍 |
| D.单位时间内生成3molA,同时生成1molB |
下列微粒之间,属于同位素的是,属于同素异形体的是,属于同分异构体的是属于同一物质的是。
| A.正丁烷与异丁烷 |
| B.红磷与白磷 |
| C.H2和D2 |
| D.石英与干冰 E. 金刚石与水晶 F. 氧气和臭氧 |
G. 13C和14C H. CH3CH2CH2CH(C2H5)CH3和 CH3CH2CH2CH(CH3)C2H5
下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白。
| ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
||
| 2 |
① |
② |
③ |
④ |
⑤ |
||||
| 3 |
⑥ |
⑦ |
⑧ |
⑨ |
|||||
(1)①②⑥⑦中原子半径最小的是(填元素符号);
(2)表中氧化性最强的单质的化学式为;
(3)这些元素的最高价氧化物的水化物中,碱性最强的是(填化学式);
(4)⑥⑦两种元素中,离子半径较小的是(填离子符号);
(5)④⑧⑨三种元素的气态氢化物的稳定性强弱顺序为>>(填化学式);
(6)表中能形成两性氢氧化物的元素是_____(填元素符号),分别写出该元素的氢氧化物与⑥、⑧的最高价氧化物对应水化物反应的化学方程式:
______________________________,_______________________________;