四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题。
| |
W |
X |
Y |
Z |
| 结构 或性质 |
最高价氧化物对应的水 化物与其气态氢化物反 应得到离子化合物 |
焰色反应呈黄色 |
在同周期主族元素形成的简单离子中,离子半径最小 |
最高正价与最 低负价之和为6 |
(1)W元素和氢可形成离子化合物,其电子式为 。
(2)Y元素和Z元素可形成YZ3化合物,可用于净水剂,净水原理 (用离子方程式表示)。
(3)①下列可作为比较X和Y金属性强弱的依据是 (填序号)。
a.最高价氧化物的水化物能反应 b.相应硫酸盐水溶液的pH
c.单质与水反应的难易程度 d.单质与酸反应时失去的电子数
②由X、Y、氢、氧四种元素所组成的化合物,能与盐酸以1:4反应生成两种常见盐和水,则该化合物的化学式为 。
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,混合后溶液中离子浓度由大到小的顺序是 。
(12分)红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如下图所示(图中的ΔH表示生成1 mol产物的数据)。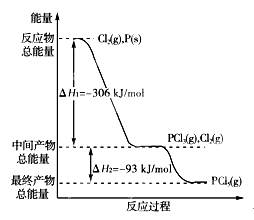
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式是
________________________________________________________________________;
(2)PCl5分解成PCl3和Cl2的热化学方程式是
________________________________________________________________________。
上述分解反应是一个可逆反应,温度T1时,在密闭容器中加入0.80 mol PCl5,反应达平衡时PCl5还剩0.60 mol,其分解率α1等于________;若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,α2________α1(填“大于”、“小于”或“等于”);
(3)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成 中间产物PCl3,然后降温,再和Cl2反应生成PCl5。原因是____________________________________________________
中间产物PCl3,然后降温,再和Cl2反应生成PCl5。原因是____________________________________________________
________________________________________________________________________
____________________________________________________________________;
(4)P和Cl2分两步反应生成1 mol PCl5的ΔH3=________,P和Cl2一步反应生成1 mol PCl5的ΔH4______ΔH3(填“大于”、“小于”或“等于”);
(5)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是_________________________________。
有一个食品广告称:“我公司生产的新型糕点不含糖,是糖尿病人的最佳选择”。下表是其包装袋上的说明,从表中的配料中分别选出一种物质填在相应的横线上。
| 品名 |
XXX |
| 配料 |
鲜鸡蛋,精面粉,精炼植物油,碳酸氢钠, 甜蜜素,柠檬黄,苯甲酸钠等 |
| 保质期 |
120天 |
| 生产日期 |
标于包装袋封口上 |
(1)富含油脂的是_____________________
(2)富含糖类的是______________________
(3)富含蛋白质的是____________________
(4)属于防腐剂的是___________________
(5)属于着色剂的是__________________
(6)属于调味剂的是____________________
(7)属于疏松剂的是___________________
(8)请分析广告的说法是否科学?____________(填“是”或“否”)
淀粉和纤维素的分子组成都可以用通式 _____表示,但二者的n值是_____的(填“相同”或“不同”)。它们都属于_____糖,在性质上跟单糖、二糖不同,没有_____味,都_____发生(填“能”或“不能”)发生银镜反应,但稀硫酸的催化作用下,都能发生_____反应。
在25℃时,向100ml含氯化氢14.6g的盐酸溶液里放人5.60g纯铁粉(不考虑反应前后溶液体积变化),反应开始至2min末,收集到1.12L(标准状况)氢气。在此之后,又经过4min,铁粉完全溶解。则:
(1)在前2min内用FeCl2表示的平均化学反应速率是_______
(2)在后4min内用HCl表示的平均化学反应速率是_______
(3)前2min与后4min相比,反应速率较快的是 ________,其原因是_____
写出常温时,下列反应的热化学方程式:
(1)3molNO2(g)与1mol H2O(l)反应生成HNO3(aq)和NO(g),放热138kJ。
(2)用CO还原1mol Fe2O3,放热24.8 kJ。
(3)1molHgO(S)分解为液态汞和氧气,吸热90.7 kJ。
(4)0.2mol NaOH与稀H2SO4完全反应放热11.46 kJ,写出表示酸与碱反应中和热的热化学方程式:
(5)0.1g H2完全燃烧放出热量12.1 kJ,写出表示H2燃烧热的热化学方程式: