已知:N2(g)+3H2(g) 2NH3(l)△H=﹣132kJ/mol,蒸发1mol NH3(l)需要吸收的能量为20kJ,相关数据如下
2NH3(l)△H=﹣132kJ/mol,蒸发1mol NH3(l)需要吸收的能量为20kJ,相关数据如下
| |
H2(g) |
N2(g) |
NH3(g) |
| 1mol分子中的化学键形成时要释放出的能量/kJ |
436 |
946 |
a |
一定条件下,在体积1L的密闭容器中加入1molN2(g)和3molH2(g)充分反应,生成NH3(g)放出热量QkJ,下列说法正确的是
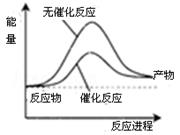
A.上图可表示合成氨过程中的能量变化
B.a的数值为1173
C.Q的数值为92
D.其它条件相同,反应使用催化剂时释放出的能量大于无催化剂时释放出的能量
下列有关离子方程式书写错误的是:
| A.将标准状况下1.12 L氯气通入10 mL 1 mol / L的溴化亚铁溶液中:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 |
| B.向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++ HCO3- +OH-=CaCO3↓+H2O |
| C.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+H++ SO42- + NH4+=BaSO4↓+ NH3·H2O +H2O |
| D.向NaHSO3溶液中滴入适量NaClO溶液:HSO3–+ ClO–=SO42–+ H+ + Cl– |
为了验证Fe3+的性质,某化学兴趣小组设计了下图所示的一组实验,其中实验方案设计错误的是: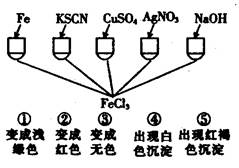
| A.只有④ |
| B.只有③ |
| C.③和④均错 |
| D.全部错误 |
下列各组离子中,一定能在指定溶液中大量共存的是:
| A.澄清透明的无色溶液:ClO-、CrO42-、Al3+、SO42- |
| B.能使pH试纸变深蓝色的溶液:Na+、AlO2-、S2-、CO32- |
| C.常温呈中性的溶液中:Fe3+、K+、Cl-、SO42- |
| D.能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32- |
关于下列各装置图的叙述中,不正确的是: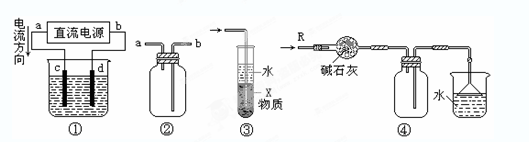
| A.装置①中,c为阳极、d为阴极 |
| B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体,且从a口进气 |
| C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 |
| D.装置④可用于干燥、收集氨气,并吸收多余的氨气 |
“拟晶”(quasicrystal)是一种具有凸多面体规则外形但不同于晶体的固态物质。A165Cu23Fel2是二十世纪发现的几百种拟晶之一,具有合金的某些优良物理性能。有关这种拟晶的说法错误的是:
| A.A165Cu23Fel2的硬度比金属A1、Cu、Fe都大 |
| B.A165Cu23Fel2中三种金属的化合价均可视作零 |
| C.A165Cu23Fel2不可用作长期浸泡在海水中的材料 |
| D.1mol A165Cu23Fel2溶于过量的硝酸时共失去265 mol电子 |