如图所示电化学装置,X可能为“锌棒”或“碳棒”,下列叙述错误的是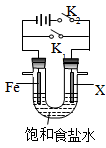
| A.X为锌棒,仅闭合K1,Fe电极上发生还原反应 |
| B.X为锌棒,仅闭合K1,产生微量电流方向:Fe→X |
| C.X为碳棒,仅闭合K2,该电化学保护法称为“牺牲阳极阴极保护法” |
| D.若X为碳棒,仅闭合K1,铁电极的极反应为:Fe -2e- → Fe2+ |
把等物质的量金属钠进行下列实验,其中生成氢气最多的是()D
| A.把钠放入足量稀盐酸中 |
| B.把钠放入足量水中 |
| C.把钠放入硫酸铜溶液中 |
| D.将钠用铝箔包好并刺些小孔,再放入水中 |
除去Na2CO3固体中少量的NaHCO3固体最佳方法是( C)
| A.加入适量盐酸 | B.加入NaOH溶液 |
| C.加热灼烧 | D.配成溶液后通入过量的CO2 |
下列变化需要加入氧化剂才能实现的是()
| A.S2-→S | B.HCO3-→CO2 | C.2 Cl-→Cl2 | D.Cu2+→Cu |
下列叙述正确的是()
①2mol铁原子 ②1mol Fe3+ ③0.5mol 氧
④0.5mol 氮气⑤氨的摩尔质量是17g
| A.①③④ | B.①②④⑤ | C.①②④ | D.都正确 |
用NA表示阿伏加德罗常数,下列叙述正确的是()
| A.64g SO2含有硫原子数为1NA | B.常温常压下,2molH2的体积是44.8L |
| C.标准状况下,22.4L H2O的分子数为1NA | D.14g N2含有分子数为0.5NA |