(本题共14分)在实验室里制取的乙烯中常混有少量的二氧化硫,某化学兴趣小组设计了如图所示的实验装置以确认上述混合气体中是否含有SO2和C2H4。请回答下列问题:

I、II、Ill、IV装置可盛放的试剂是:(请将下列有关试剂的序号填入对应装置内,可重复选用)。
| A.品红溶液 | B.NaOH溶液 | C.浓硫酸 | D.溴水 |
I ; IV ;
能说明SO2气体存在的现象是 ;使用装置Ⅱ的目的是 ;
确定含有乙烯的现象是 ;
酯的制备是重要的有机化学实验,甲、乙同学分别使用图1、图2装置制取乙酸乙酯。

甲同学在制得乙酸乙酯后,将乙酸乙酯与饱和碳酸钠溶液分离的仪器是__________。
图1导管末端不能插入饱和碳酸钠溶液,而图2装置中的仪器C的末端可以插入饱和碳酸钠溶液的是因为该装置具有 功能。
现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物,下列框图是分离操作步骤流程图:

则试剂a是__________,分离方法Ⅱ是____________。
测定乙酸乙酯的纯度:取乙同学所得乙酸乙酯样品1.0 g,放入20.00 mL 0.500 mol.L-1的NaOH溶液中,充分振荡四小时,滴入两滴酚酞后,用0.075 mol·L-1的盐酸标准溶液滴定,重复三次实验测得盐酸用量的平均值为20.00 mL。该乙酸乙酯样品的纯度为 。
(已知:CH3COOC2H5+NaOH==CH3COONa+C2H5OH)
某固体混合物可能含有 、
、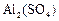 、
、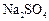 、
、 、
、 和
和 。将该混合物进行如下实验,根据所给实验现象完成表格(对于能确定的物质在相应位置写化学式,暂不能确定的物质在相应位置填“无”) :.
。将该混合物进行如下实验,根据所给实验现象完成表格(对于能确定的物质在相应位置写化学式,暂不能确定的物质在相应位置填“无”) :.
(1)将少许混合物放入水中得到无色溶液和白色沉淀。
| 肯定存在的物质 |
肯定不存在的物质 |
理由 |
(2)取溶液进行焰色反应,火焰呈黄色。
| 肯定存在的物质 |
肯定不存在的物质 |
理由 |
(3)取白色沉淀加入稀盐酸,沉淀完全溶解并放出气体。
| 肯定存在的物质 |
肯定不存在的物质 |
理由 |
(4)通过上述实验仍无法确定的物质是。
下图是实验室制取Cl2并以Cl2为原料进行特定反应的实验: 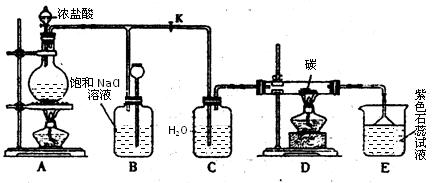
(1)A为氯气发生装置,写出反应的化学方程式________________________。
(2)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C瓶后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl,写出D装置中反应的化学方程式 _____;装置C的作用是 。
(3)E处石蕊试液的现象是_______________;其原因是__________________。
(4)若将E处溶液改为石灰水,反应过程的现象是_____________________________。
A.有白色沉淀生成
B.无白色沉淀生成
C.先生成白色沉淀,然后沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此处B中的现象是________________,B的作用是________________。
[化学选修──有机化学基础]
根据图示回答下列问题:
(1)写出A、E、G的结构简式:A_____________,E_______________,G______________;
(2)反应②的化学方程式(包括反应条件)是_________________________,
(3)反应④化学方程式(包括反应条件)是______________________ ______________;
(4)写出①、⑤的反应类型:①________________、⑤__________________。
为研究铁质材料与热浓硫酸的反应,某小组进行了以下探究活动:
[探究一]
(1)称取铁钉(碳素钢)12.0g放入30.0mL浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除Fe3+外还可能含有Fe2+。若要确认其中是否含有Fe2+,应选择加入的试剂为____(选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液
c.浓氨水 d.酸性KMnO4溶液
②乙同学取672 mL(标准状况)气体Y通入足量溴水中,发生反应:
SO2+Br2+2H2O=2HBr+H2SO4
然后加入足量BaCl2溶液,经适当操作后得到干燥固体4.66g。据此推知气体Y中SO2的体积分数为____。(相对原子质量:O—16 S—32 Ba—137)
[探究二]
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含量有H2和CO2气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
(2)写出产生CO2的化学方程式____。
(3)装置A中试剂的作用是____。
(4)简述确认气体Y中含有CO2的实验现象。
(5)如果气体Y中含有H2,预计实验现象应是。
下图中A~J均代表无机物或其水溶液,其中A是一种红棕色粉末,B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料。
根据图示回答问题:
(1)写出下列物质的化学式:A ,E,I;
(2)反应①的化学方程式是;
反应②的化学方程式是;
(3)J与盐酸反应的离子方程式是;
反应后的溶液与D反应的化学方程式是。