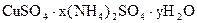(本题共14分)中学化学中有许多与氮有关的反应。阅读材料,回答问题。
氨气和氧气在催化剂存在下的反应方程式为4NH3十5O2→4NO+6H2O完成下列计算:
①生成1molNO消耗氧气的体积为 L(标准状况)。
②5 mol NH3和5 molO2反应生成4 molNO,过量的氨溶于产物水中成为氨水,所得氨水的密度为0.75g/ml,则该氨水的物质的量浓度为_____mol/L。
③.如果没有催化剂,氨氧化生成NO的同时也生成氮气:4NH3十3O2→2N2+6H2O。若4 mol NH3和4 molO2恰好完全反应,则产物气体中NO的物质的量为_____ mol。
已知真空管中反应2NO2
 N2O4,现向一真空管中充入4L标况下的NO2气体:
N2O4,现向一真空管中充入4L标况下的NO2气体:
① 若在上述反应中有50% NO2的转化为N2O4,所得混合气的平均摩尔质量为______g/mol
若在上述反应中有50% NO2的转化为N2O4,所得混合气的平均摩尔质量为______g/mol (保留一位小数)。
(保留一位小数)。
② 将4LNO2通过真空管反应后,恢复到原状况,得到气体3L,其中NO2为_______L。
将4LNO2通过真空管反应后,恢复到原状况,得到气体3L,其中NO2为_______L。
各种氮氧化物(NO、NO2)是主要的大气污染物之一,治理氮氧化物(NOX)废气的方法之一是用NaOH溶液进行吸收,其反应原理可表示如下:
NO2+NO+2NaOH→2NaNO2+H2O 2NO2+2NaOH→ NaNO2+NaNO3+H2O
现有一NO与NO2的混合气体,将其通入50mL 2mol/L的NaOH溶液中,恰好完全吸收,测得溶液中含有NO3―0.02mol。
①所得溶液中NaNO2的物质的量为 mol;②混合气体中V(NO):V(NO2)= 。
在150 mL 0.2 mol·L-1硫酸铜溶液中插入两个电极,通电电解(不考虑水的电解),则:
(1)若两极均为铜片,试说明电解过程中Cu2+浓度将怎样变化。_____________________。
(2)若阳极为纯锌,阴极为铜片,阳极的电极反应式是______________________________。
(3)如不考虑H+在阴极上放电,当电路中有0.04 mol e-通过时,阴极增重________g,阴极上的电极反应式是___________________________。
1 mol的某有机物甲在O2中充分燃烧,可得到相同条件下等体积的CO2和H2O(g),并消耗112L(标准状况)O2;又知甲的相对分子质量小于100,1 mol甲在酸性条件下可水解生成1 mol乙和1 mol丙,且丙通过一定途径可转化为乙。
(1)甲的分子式为 。
(2)与甲分子式、所属物质类别都相同的有机物的同分异构体有 种(不含甲)。
|
已知:①ROH+HBr(氢溴酸)→ RBr+H2O
|
|
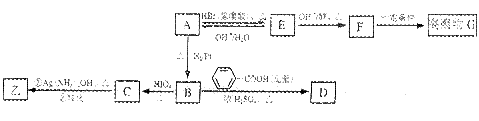 A与甲为同分异构体,且A中含有碳氧双键,B只生成C,与A相关的反应如下:
A与甲为同分异构体,且A中含有碳氧双键,B只生成C,与A相关的反应如下:
某烃A相对分子质量是156,在CCl4溶液中跟Br2不起反应,但在光照下,Br2可以跟A起取代反应,取代产物的相对分子质量是235的有两种:产量较多的一种是B,产量较少的一种是C。另外,还可得到相对分子质量是314的产物多种。
(1)请写出A、B、C的结构简式。
(2)相对分子质量是314的有多少种?
常温下,一种烷烃A和一种烯烃B组成的混合气体。A和B分子最多只含有4个碳原子,且B分子的碳原子数比A分子的多。
(1)将1 L该混合气体充分燃烧,在同温、同压下得到2.5 L CO2气体。试推断原混合气体中A和B所有可能的组合及其体积比,并将结论填入下表。
| 组合编号 |
A的分子式 |
B的分子式 |
A和B的体积比V(A)∶V(B) |
(2)120 ℃时取1 L该混合气体与9 L O2混合,充分燃烧,当恢复到120 ℃和燃烧前的压强时,体积增大6.25%。试通过计算确定A和B的分子式。