用NA表示阿伏德罗常数,下列叙述正确的是
| A.标准状况下,22.4LH2O含有的分子数为1 NA |
| B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| C.通常状况下,1 NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5mol·/L的MgCl2溶液中,含有Cl-个数为1 NA |
有Fe2+、NO3-、Fe3+、NH4+、H+ 和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述错误的是
| A.氧化剂与还原剂的物质的量之比为8:l |
| B.还原产物为NH4+ |
| C.若有l mol NO3-参加还原反应,则转移8mol e- |
| D.若把该反应设计为原电池,则负极反应为Fe 2+ -e-=Fe 3+ |
将51.2g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.9 mol,这些气体恰好能被500ml、2 mol/LNaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO3的物质的量为()
mol/LNaOH溶液完全吸收,生成含NaNO3和NaNO2的盐溶液,其中NaNO3的物质的量为()
| A.0.2mol | B.0.4mol | C.0.8mol | D.0.9mol |
中学阶级介绍的应用电解法制备的物质主要有三种:一是铝的工业制备、二是氯碱工业、三是金属钠的制备。下列关于这三个工业生产的描述中正确的是
A.电解法制金属钠时,负极反应式:Na + + e-=" Na" + + e-=" Na" |
| B.电解法生产铝时,需对铝土矿进行提纯,在提纯过程中应用了氧化铝或氢氧化铝的两性 |
| C.在氯碱工业中,电解池中的阴极产生的是 H2,NaOH 在阳极附近产生 |
| D.氯碱工业和金属钠的冶炼都用到了NaCl ,在电解时它们的阴极都是 C1一失电子 |
现有用离子交换膜(只允许对应的离子通过)和石墨作电极的电解槽电解饱 和的Na2SO4溶液生产NaOH和H2SO4,下列说法中正确的是
和的Na2SO4溶液生产NaOH和H2SO4,下列说法中正确的是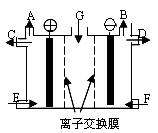
| A.气体A是H2 ,溶液E是稀硫酸 |
| B.气体B是H2 ,溶液D是NaOH溶液 |
| C.Na2SO4溶液由G口加入,F口加入稀硫酸 |
| D.靠阳极室一侧的是阳离子交换膜,阴极室导出的是氢气 |
从下列事实所列出的相应结论正确的是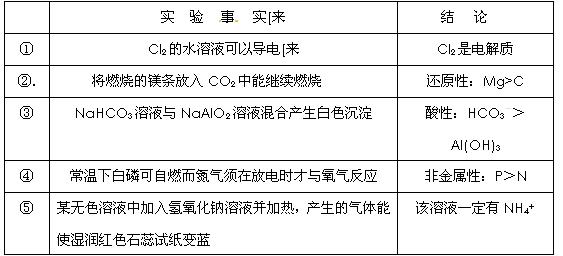
| A.③④⑤ | B.①②③ | C.②③⑤ | D.全部 |