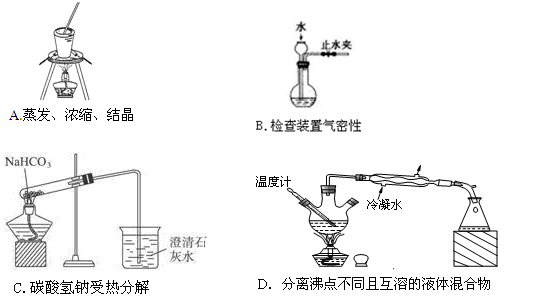
用下图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是
| 选项 |
①中物质 |
②中物质 |
预测②中的现象 |
| A. |
稀盐酸 |
碳酸钠与氢氧化钠的混合溶液 |
立即产生气泡 |
| B. |
浓硝酸 |
用砂纸打磨过的铝条 |
产生红棕色气体 |
| C. |
新制氯水 |
淀粉碘化钾溶液 |
溶液变蓝色 |
| D. |
浓盐酸 |
二氧化锰 |
产生黄绿色气体 |
由一种阳离子和两种酸根离子组成的盐称混盐。下列关于混盐Na4S2O3的有关判断,不正确的是
| A.该混盐水溶液呈碱性 |
| B.该混盐与H2SO4反应有气体生成 |
| C.该混盐溶液加入BaCl2可以生成白色沉淀 |
| D.该混盐在酸性条件下可生成S,每产生32g S转移2NA个电子 |
已知某有机物X的结构简式如图所示,下列有关叙述不正确的是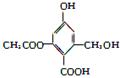
| A.X的化学式为C10H10O6 |
| B.X在一定条件下能与FeCl3溶液发生显色反应 |
| C.1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol |
| D.X在一定条件下能发生消去反应和酯化反应 |
下列说法正确的是
| A.电解法精炼铜,当阴极质量增加32 g时,一定有6.02×1023个电子转移 |
| B.含10.6 g Na2CO3的溶液中,所含阴离子总数等于6.02×1022 |
| C.28 g由乙烯和氮气组成的混合气体中,含有6.02×1023个原子 |
| D.含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为6.02×1022 |
下列解释实验事实的方程式正确的是
| A.Al2(SO4)3溶液滴加氨水产生白色胶状沉淀:Al3+ + 3OH-= Al(OH)3 ↓ |
B.90℃时测得纯水中c(H+)·c(OH-) =3.8×10-13:H2O(l) H+(aq) + OH-(aq) △H<0 H+(aq) + OH-(aq) △H<0 |
| C.FeCl3溶液中通入SO2,溶液黄色褪去:2Fe3++SO2 +2H2O = 2Fe2+ + SO42-+ 4H+ |
D.碳酸钠溶液滴入酚酞变红:CO32-+ 2H2O  H2CO3 + 2OH- H2CO3 + 2OH- |
下列实验正确的是: