相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g) 2XY3(g)△H=-92.6kJ·mol-1
2XY3(g)△H=-92.6kJ·mol-1
起始时各物质物质的量如下表所示:
| 容器 |
起始时各物质物质的量/mol |
||
| X2 |
Y2 |
XY3 |
|
| ① |
1 |
3 |
0 |
| ② |
0.6 |
1.8 |
0.8 |
达到平衡后,①容器中XY3的物质的量为0.5mol。下列叙述正确的是
A.容器①、②中反应的平衡常数不相等
B.达平衡时,容器②中XY3的物质的量浓度为2mol·L—1
C.容器①中反应达到平衡时放出的热量为23.15 kJ
D.容器②中反应达到平衡时放出热量
可以验证硫元素的非金属性比氯元素弱的事实是( )
①H2S水溶液是弱酸,HCl水溶液是强酸
②向氢硫酸溶液中滴入氯水有单质硫生成
③硫、氯气分别与铜和铁反应,其产物是FeS、Cu2S、FeCl3、CuCl2
④高氯酸(HClO4)的酸性比硫酸强
| A.②③④ | B.②④ | C.①②④ | D.①②③④ |
2011年3月11日,日本本州岛仙台港发生9.0级地震,地震引发海啸、食盐、蔗糖、醋酸、“84消毒液”、明矾等是灾后居民日常生活中经常使用的物质,下列有关说法或表示正确的是( )
A.食盐中阴离子的结构示意图为: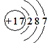 |
| B.蔗糖和醋酸都是弱电解质 |
C.“84消毒液”中有效成分NaClO的电子式为: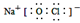 |
| D.明矾溶液水解可制得Al(OH)3胶体,用于杀菌消毒 |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只能被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果错误的是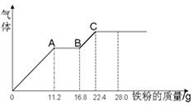
| A.原混合液中NO3-的物质的量为0.2mol |
| B.OA段产生是NO,AB段反应为2Fe3++Fe = 3Fe2+,BC段产生氢气 |
| C.溶液中最终溶质为FeSO4 |
| D.c(H2SO4)为5mol·L-1 |
海带中含有碘离子,某化学兴趣小组设计如下的步骤从海带中提取单质碘:
①通足量氯气 ②将海带烧成灰,向灰中加水搅拌
③加CCl4振荡 ④过滤 ⑤用分液漏斗分液。
合理的操作顺序为
| A.①→③→⑤→②→④ | B.②→①→③→④→⑤ |
| C.②→④→①→③→⑤ | D.③→①→②→⑤→④ |
将表面有少量氧化铜的铜片,和铁片同时加入足量稀盐酸中,经充分反应后,溶液中一定含有的金属离子是
| A.Fe2+ | B.Fe2+和Cu2+ | C.Fe3+和Cu2+ | D.Fe2+和Fe3+ |