广州地区的自来水是采用氯气消毒的,为了检验Cl-的存在,最好选用下列物质中的
| A.石蕊溶液 | B.四氯化碳 | C.氢氧化钠溶液 | D.硝酸银溶液 |
目前已研制成功多种锂电池。某种锂电池的总反应式为Li+MnO2=LiMnO2,下列说法正确的是( )。
| A.Li是正极,电极反应为Li-e-=Li+ |
| B.Li是负极,电极反应为Li-e-=Li+ |
C.Li是负极,电极反应为MnO2+e-=Mn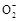 |
| D.Li是负极,电极反应为Li-2e-=Li2+ |
据媒体报道,以氢氧燃料电池为动力的公交车即将在北京试运行。质子交换膜燃料电池(PEMFC)常作为电动汽车的动力源。该燃料电池以氢气为燃料,空气为氧化剂,铂作催化剂,导电离子是H+。下列对该燃料电池的描述中正确的是( )。
①正极反应为O2+4H++4e-=2H2O
②负极反应为2H2-4e-=4H+
③总的化学反应为2H2+O2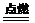 2H2O
2H2O
④氢离子通过电解质向正极移动
A.①②③ B.②③④ C.①②④ D.①②③④
如将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即构成甲烷燃料电池。已知通入甲烷的一极,其电极反应为CH4+10OH--8e-=C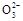 +7H2O,下列叙述正确的是( )。
+7H2O,下列叙述正确的是( )。
| A.通入甲烷的一极为正极 |
| B.通入氧气的一极发生氧化反应 |
C.该电池总反应为CH4+2O2+2OH-=C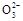 +3H2O +3H2O |
| D.该电池在工作时,溶液中的阴离子向正极移动 |
下列说法正确的是( )。
| A.构成原电池正极和负极的材料必须是金属 |
| B.在原电池中,电子流出的一极是负极,该电极被还原 |
| C.实验室欲快速制取氢气,可利用粗锌与稀硫酸反应 |
| D.原电池可以把物质内部的能量全部转化为电能 |
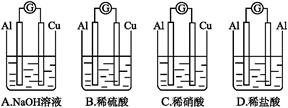
为将反应2Al+6H+=2Al3++3H2↑的化学能转化为电能,下列装置能达到目的的是(铝条均已除去了氧化膜)( )。