用下列实验装置进行相应实验,能达到实验目的的是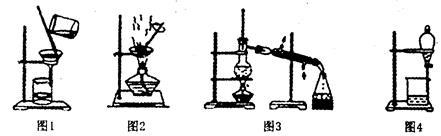
| A.用图1所示装置从Fe(OH)3胶体中过滤出Fe(OH)3胶粒 |
| B.用图2所示装置蒸发CuCl2溶液制得CuCl2晶体 |
| C.用图3所示装置可由自来水制得蒸馏水 |
| D.用图4所示装置从C2H5OH与C2H5COOCCH3,的混合物中分离出乙酸乙酯 |
已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO3―+ H2O H2SO3 + OH― ① HSO3―
H2SO3 + OH― ① HSO3― H+ + SO32― ②
H+ + SO32― ②
向0.1 mol · L -1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是
| A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3―)增大 |
B.加入少量Na2SO3固体,则c(H+) + c(Na+) = c(HSO3―) + c(OH―) +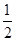 c(SO32―) c(SO32―) |
C.加入少量NaOH溶液,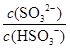 、 、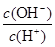 的值均增大 的值均增大 |
| D.加入氨水至中性,则2c(Na+) = c(SO32―)>c(H+) = c(OH―) |
下图表示溶液中c(H+)和c(OH-)关系,下列判断错误的是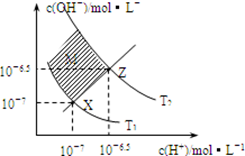
| A.两条曲线间任意点均有c(H+)×c(OH-)=Kw |
| B.M区域内任意点均有c(H+)<c(OH-) |
| C.图中T1<T2 |
| D.XZ线上任意点均有pH=7 |
某酸的酸式盐NaHY的水溶液显碱性,下列有关叙述正确的是 ( )
A.H2Y的电离方程式为:H2Y 2H++Y2— 2H++Y2— |
| B.在该盐的溶液里,离子浓度为:c(Na+)>c(Y2—)>c(HY—)>c(OH—)>c(H+) |
| C.在该盐的溶液里,离子浓度为:c(Na+)>c(HY—)> c(OH-)> c(Y2—) |
D.HY—水解方程式为:HY—+H2O H3O++ Y2— H3O++ Y2— |
实验测得常温下 某一元酸(HA)溶液pH≠1,
某一元酸(HA)溶液pH≠1, 某一元碱(BOH)溶液里
某一元碱(BOH)溶液里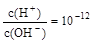 ,将这两种溶液等体积混合,所得溶液各离子物质的量浓度由大到小顺序是( )
,将这两种溶液等体积混合,所得溶液各离子物质的量浓度由大到小顺序是( )
A.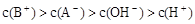 B.
B.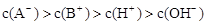
C. D.
D.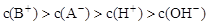
在25 mL 0.1 mol/L NaOH溶液中逐滴加入0.2 mol/L CH3COOH 溶液,曲线如下图所示,有关粒子浓度关系比较正确的()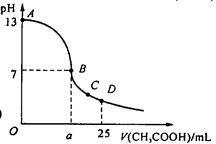
A.在A、B间任一点,溶液中一定都有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)= c(H+)
C.在C点:c(Na+)>c(CH3COO-) >c(H+)>c(OH-)
D.在D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)