为验证氧化性Cl2>Fe3+> SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。

实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的离子。
V.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程I的目的是____。
(2)检验B中溶液是否还有Fe2+的方法之一是:取少量B中溶液于试管中,滴加几滴含有+3价铁元素的配合物溶液,会产生蓝色沉淀.写出该反应的离子方程式____ 。
(3)若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的离子方程式____。
(4)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的化学方程式为________。
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定不能够证明氧化性Cl2>Fe3+>SO2的是____(填“甲”、“乙”或“丙”)。
| |
过程Ⅳ,B溶液中含有的离子 |
过程Ⅵ,B溶液中 含有的离子 |
| 甲 |
有Fe3+无Fe2+ |
有SO42- |
| 乙 |
既有Fe3+又有Fe2+ |
有SO42- |
| 丙 |
有Fe3+无Fe2+ |
有Fe2+ |
(6)将B中的FeCl2溶液换成100 mLFeBr2溶液并向其中通入1.12 LCl2(标准状况下),若溶液中有1/2的Br一被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为____ mol/L。
实验室欲配制0.5 mol/L的NaOH溶液500 mL,有以下仪器:①烧杯②玻璃棒③托盘天平(带砝码)④药匙,按要求填空:
(1)配制时,需称取NaOH的质量是g,还缺少的仪器是
。
(2)使用容量瓶前必须进行的一步操作是。
(3)在配制过程中,其他操作都正确的情况下,下列操作会导致所配制的溶液浓度偏高的是。(选填序号)
①没有洗涤烧杯和玻璃棒②未等NaOH溶液冷却至室温就转移到容量中
③容量瓶不干燥,含有少量蒸馏水④定容时仰视标线⑤定容时俯视标线
实验室常用苯甲醛在浓氢氧化钠溶液中制备苯甲醇和苯甲酸,反应式如下:
已知:①苯甲酸在水中的溶解度为:0.18g(4℃)、0.34g(25℃)、0.95g(60℃)、6.8g(95℃)
②乙醚沸点34.6℃,密度0.7138,易燃烧,当空气中含量为1.83%~48.0%时易发生爆炸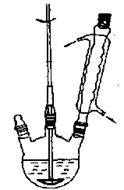

图1制备苯甲酸和苯甲醇的反应装置图图2蒸乙醚的装置图
实验步骤如下:
①向图1所示装置中加入8g氢氧化钠和30mL水,搅拌溶解。稍冷,加入10 mL新蒸过的苯甲醛。开启搅拌器,调整转速,使搅拌平稳进行。加热回流约40 min。
②停止加热,从球形冷凝管上口缓缓加入冷水20mL,摇动均匀,冷却至室温。反应物冷却至室温后,倒入分液漏斗,用乙醚萃取三次,每次10mL。水层保留待用。合并三次萃取液,依次用5 mL饱和亚硫酸氢钠溶液洗涤,10mL 10%碳酸钠溶液洗涤,10 mL水洗涤。
③分出醚层,倒入干燥的锥形瓶,加无水硫酸镁,注意锥形瓶上要加塞。将锥形瓶中溶液转入图2所示蒸馏装置,缓缓加热。升高温度蒸馏,当温度升到140℃时改用空气冷凝管,收集198℃~204℃的馏分得产品A。将萃取后的水溶液慢慢地加入到盛有30 mL浓盐酸和30 mL水的混合物中,同时用玻璃棒搅拌,析出白色固体。冷却,抽滤,得到粗产品,然后提纯得产品B。
根据以上步骤回答下列问题:
(1)步骤①中所加的苯甲醛为什么要是新蒸的?________________________________。
(2)步骤②萃取时用到的玻璃仪器除了除烧杯、玻璃棒外,还需______________________,饱和亚硫酸氢钠溶液洗涤是为了除去__________________,而碳酸钠溶液洗涤是为了除去醚层中极少量的苯甲酸。
(3)步骤③中无水硫酸镁的作用是_________________,将锥形瓶中溶液转入图2所示蒸馏装置时涉及的实验操作为__________________。
(4)产品A为____________,蒸馏除乙醚的过程中采用的加热方式为_______________,提纯产品B所用到的实验操作为________________。
Ⅰ:选择一种试剂鉴别下列各组物质,将所选试剂的化学式或名称写在横线上:
① 苯、甲苯② 苯、硝基苯、乙醇
③ 苯酚溶液、己烯、己烷、醋酸溶液
Ⅱ:为了探究苯酚和乙醇分子中羟基上氢原子的活泼性,甲、乙两位同学分别设计如下甲、乙两方案。
方案甲:
实验1:取少量无水乙醚于试管中,加入少量金属钠。
实验2:各取3mL无水乙醚于试管中,分别加入少量等物质的量的苯酚和乙醇,再投入大小相同的钠块。
方案乙:
各取少量等物质的苯酚和乙醇于试管中,均在60℃的水浴加热,待苯酚熔化后,各放入相同大小的一小块金属钠。(已知:苯酚的密度为1.07g/mL)
(1)方案甲设计实验1的目的是。
(2)方案乙中观察到:在乙醇中,钠很快与乙醇反应产生气体,溶液保持澄清;在苯酚中,钠块表面有少量气泡,且表面产生白色悬浮物,最后白色悬浮物充满苯酚熔融液。
①实验中观察到的白色悬浮物为;
②苯酚熔融液与钠的反应速率不如无水乙醇与钠的反应快,其可能原因有____________、_____________。
两位同学设计了下述两个方案, 并都认为如果观察到的现象和自己所设计的方案一致,即可确定无色气体中一定含有SO2和CO2气体。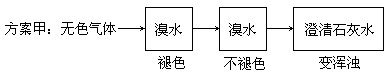
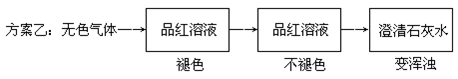
请你评价上述两个方案是否严密,并说明理由。
方案甲:_________,______________________
方案乙:_________,_______________________ 。
(1)试回答下列中学化学实验中常见仪器的有关问题:
在仪器①分液漏斗、②试剂瓶、③集气瓶、④滴瓶、⑤滴定管、⑥容量瓶、⑦量筒、⑧托盘天平中,标有“0”刻度的是(填序号,下同);标有使用温度的仪器是。用到“磨砂”处理的有。
(2)如下图是实验室制取酚醛树脂的装置图。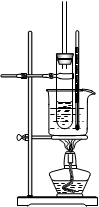
①装置中的二处错误是____________;_________。
②本实验浓盐酸作用,实验完毕后,若试管用水不易洗涤,可以加入少量_______浸泡几分钟,然后洗净。
③写出实验室制取酚醛树脂的化学方程式_______________________