下列方法中,不能用于实验室制取氨的是
| A.在烧瓶中将熟石灰和氯化铵混合,加水调成泥状后加热 |
| B.加热试管中的氯化铵固体 |
| C.将烧瓶中的浓氨水加热 |
| D.将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中 |
设NA表示阿伏加德罗常数,下列叙述中正确的是
| A.常温常压下,11.2L氧气所含的原子数为NA |
B.17g的NH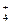 离子中含有的电子数为NA 离子中含有的电子数为NA |
| C.常温常压下,48gO3含有的氧原子数为3NA |
| D.24g金属镁变为镁离子时失去的电子数为NA |
下列数量的各物质所含的原子数按由大到小顺序排列正确的是
①0.5molNH3②标准状况下22.4L氦气(He)③4℃时9mL水④0.2molNa3PO4
| A.①③④② | B.①④③② | C.④③②① | D.②③④① |
可用离子方程式H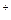 +OH
+OH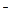 =H
=H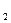 O表示的化学反应是
O表示的化学反应是
A.CH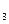 COOH+NaOH=CH COOH+NaOH=CH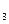 COONa+H COONa+H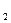 O O |
B.2HNO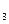 +Mg(OH) +Mg(OH)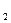 =Mg(NO =Mg(NO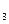 ) )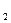 +2H +2H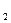 O O |
C.H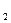 SO SO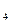 +Ba +Ba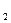 (OH) (OH)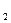 =BaSO =BaSO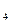 ↓+2H ↓+2H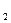 O O |
D.2HCl+Ba(OH)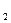 =BaCl =BaCl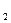 +2H +2H O O |
吸入人体內的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体內的活性氧。由此推断Na2SeO3的作用是
| A.作还原剂 | B.作氧化剂 |
| C.既作氧化剂又作还原剂 | D.既不作氧化剂又不作还原剂 |
某学生配制一定物质的量浓度的氢氧化钠溶液后,经测定发现溶液浓度偏低。该学生得出了以下原因,其中是使溶液浓度偏低的原因的是
| A.容量瓶刚用氢氧化钠溶液润洗过 |
| B.在转移溶液时不小心洒落瓶外 |
| C.在烧杯中溶解了氢氧化钠后,趁热将溶液到入容量瓶,并迅速配成了溶液 |
| D.定容时,俯视刻度线 |