“纳米技术”广泛的应用于催化及军事科学中,“纳米技术”是指粒子直径在几纳米到几十纳米的材料。如将“纳米材料”分散到液体分散剂中,所得的混合物具有的性质是( )
| A.能全部通过半透膜 | B.能发生丁达尔现象 |
| C.一定能导电 | D.一定为悬浊液或乳浊液 |
下列事实不能作为实验判断依据的是()
| A.钠和镁分别与冷水反应,判断钠和镁的金属活动性强弱 |
| B.在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属活动性强弱 |
| C.硫酸和硅酸钠溶液反应出白色沉淀,判断硫与硅的非金属活动性强弱 |
| D.Br2与I2分别与足量的H2反应,判断溴与碘的非金属活动性强弱 |
下列有关化学用语使用正确的是()
A.硫原子的原子结构示意图: |
B.NH4Cl的电子式: |
C.原子核内有10个中子的氧原子: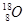 |
| D.纯碱的化学式为NaOH |
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是()
| A.原子半径:W>Z>Y>X>M |
| B.XZ2、M2Z2、W2Z2均为含非极性键的共价化合物 |
| C.由X元素形成的单质有的可以导电 |
| D.由X、Y、Z、M四种元素形成的化合物中不可能含有离子键 |
下列各组物质中,化学键的类型相同的是( )
| A.CaCl2和Na2S | B.Na2O和Na2O2 |
| C.N2和Ne | D.HCl和NaOH |
以下说法正确的是( )
| A.共价化合物内部可能有极性键和非极性键 |
| B.原子或离子间相互的吸引力叫化学键 |
| C.非金属元素间只能形成共价键 |
| D.金属元素与非金属元素的原子间只形成离子键 |