用元素符号或化学式填空:
(1)空气中含量第二的气体
(2)钙元素
(3)二氧化硫
(4)干冰是由 元素组成
用化学符号表示:
⑴铜元素 ⑵三个钾原子 ⑶氦气
⑷两个二氧化碳分子⑸ 3个硫酸根离子____________
写出下列符号的意义
2N___________ 4O2__________ Ne Ca2+ 2Cl-
(共6分)下图中, 表示氧原子,
表示氧原子, 表示氢原子。
表示氢原子。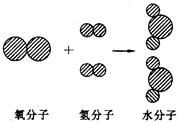
(1)根据此图,试各说出一种观点
a从物质组成的角度、说说水的组成_____________________________________;
b从分子构成的角度、说说水分子的构成_________________________________________。
(2)根据此图,从“分子—原子层面”说说化学反应的本质:
(3)此化学反应的表达式___________________________、化学反应基本类型为____________
已知“○”、“●”表示质子数不同的原子。
(1)下列表示的物质中,属于化合物的是
(2)下列表示的物质中,属于混合物的是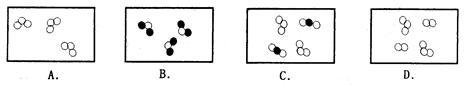
下图表示的是物质与其构成微粒之间的关系,“→”表示“构成”。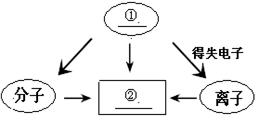
填写图中空白:①_________,②_________。