下列离子方程式正确的是
| A.用碘酸钾氧化酸性溶液中的碘化钾:5I-+IO-3+3H2O=3I2+6OH- |
| B.向H218O中投入Na2O2固体: 2H218O + 2Na2O2=4Na++ 4OH-+18O2↑ |
| C.在100 mL 2 mol/L FeBr2溶液中通入4.48 L氯气(标况下),充分反应:2Fe2++ 2Br-+ 2Cl2= 2Fe3+ + Br2+4Cl- |
| D.金属钠投入水中:Na+H2O = Na++OH-+H2↑ |
室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
下列判断不正确的是()
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后溶液中:c(OH-)=c(K+)-c(A-)=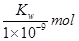 ·L-1
·L-1
C.实验②反应后的溶液中:c(A-)+c(HA) 0.1mol·L-l
0.1mol·L-l
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+)
香花石被誉为“矿石熊猫”,由我国地质学家首次发现,它由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是:()
| A.原子半径:Y>Z>R>T |
| B.气态氢化物的稳定性:W<R<T |
| C.最高价氧化物对应的水化物碱性:X>Z |
| D.XR2、WR2两化合物中R的化合价相同 |
中科院化学所研制的晶体材料——纳米四氧化三铁,在核磁共振造影及医药上有广泛用途,其生产过程的部分流程如图所示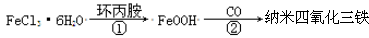
下列有关叙述不合理的是()
| A.纳米四氧化三铁可分散在水中,它与FeCl3溶液的分散质直径相当 |
| B.纳米四氧化三铁具有磁性,可作为药物载体用于治疗疾病 |
| C.在反应①中环丙胺的作用可能是促进氯化铁水解 |
| D.反应②的化学方程式是6FeOOH +CO |
化学与生活、生产、社会密切相关。下列说法正确的是()
| A.高纯度的单晶硅用于制造登月车的光电池和光导纤维 |
| B.棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2O |
| C.加碘食盐能使淀粉溶液变蓝 |
| D.有些肾病患者要定期进行血透,血透原理是利用渗析的方法净化血液 |
对盆栽鲜花施用S-诱抗素制剂,可以保持鲜花盛开。S-诱抗素的分子结构如图,则1mol该物质与足量的NaOH溶液反应时最多可消耗NaOH的物质的量为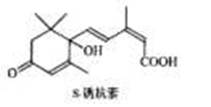
| A.1mol | B.2mol | C.3mol | D.4mol |