现有五种物质A、B、C、D、E,其中有一种是碱,四种是盐,溶于水后电离可以产生下表中的离子: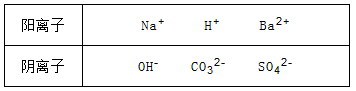
为鉴别它们,分别完成以下实验,其结果如下:
①A 溶液与B 溶液反 应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B 溶液与 C 溶液反应生成白色沉淀 D,沉淀 D 不溶于稀硝酸。
请根据上述实验结果,填空:
(1)写出下列物质的名称:X____________________。
(2)鉴别B在溶液中产生的阴离子的实验操作方法是______________________。
(3)完成以下水溶液中的反应的化学方程式:
A溶液与B溶液反应:_____________________
B溶液与E沉淀反应:_____________________
B与 C 反应至溶液呈中性:_____________________
(4)D 与 E 的混合物 ag,加入足量盐酸,反应完毕生成标准状况时的气体 bL,则D在混合物中的质量分数为___________________________。
通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的的质量确定有机物的组成。下图所示的是用燃烧法确定有机物分子式的常用装置。 现准确称取一定量某烃样品,经燃烧后A管增重2.2 g, B管增重1.08g。请回答:
现准确称取一定量某烃样品,经燃烧后A管增重2.2 g, B管增重1.08g。请回答:
(1)按上述所给的测量信息,装置的连接顺序应是:D
(2)C管中浓硫酸的作用是
(3)该有机物在纯氧中充分燃烧的化学方程式为(有机物用分子式表示)
(4)若该有机物分子中含有4个甲基,则该有机物的结构简式为
I.肼(N2H4)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。 已知在25℃、l0lkPA时,16gN2H4在氧气中完全燃烧生成氮气和H2O,放出热量312kJ。
(1)该条件下,N2H4完全燃烧的热化学方程式为
(2)传统制备肼的方法是以NAClO氧化NH3,制得肼的稀溶液,该反应的方程式为
II.钢铁工业是国家工业的基础。请回答钢铁腐蚀、防护过程中的有关问题。
(1)铁在潮湿的空气中容易被腐蚀,写出铁发生电化学腐蚀时,负极的电极反应式
(2)下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。图中A、B、C、D四个区域,生成铁锈最多的是(填字母)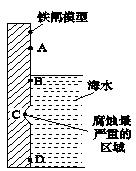
(3)下列各个装置中铁棒被腐蚀由难到易的顺序是______(填字母)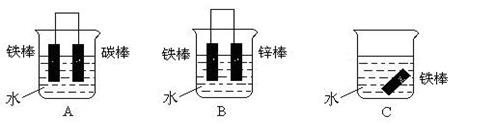
有A、B、C、D四种元素,它们均为短周期元素。已知A是非金属性最强的元素,且D与A同族;金属B的原子核内质子数比前一周期的同族元素多8,其单质不能从CuSO4溶液中置换出Cu;C元素有三种同位素,Cl、C2、C3,C1的质量数分别为C2、C3的1/2和1/3 。
(1)写出A元素的离子结构示意图
(2)C、D两种元素形成化合物的电子式
(3)写出B投入硫酸铜溶液中发生反应的化学方程式
(8分)698 K时,向某V L的密闭容器中充入2 mol H2(g)和2 mol I2(g),发生反应:H2(g)+I2(g) = 2HI(g),测得各物质的物质的量浓度与时间变化的关系如图所示。
请回答下列问题:
(1)容器的体积V=_____L
(2)反应达到最大限度的时间是__s,该时间内平均反应速率v(HI)=mol·L-1·s-1
(3)判断该反应达到平衡的依据是(填序号)
① (I2)=2
(I2)=2 (HI)
(HI)
②H2、I2、HI的浓度都不变
③容器内气体的压强保持不变
④容器内气体的密度保持不变
下图是某兴趣小组探究不同条件下化学能转变为电能的装置
(1)当电极A为Fe、电极B为Cu、电解质溶液为硫酸铜溶液时,正极的电极反应式为
(2)当电极A吸附CH4、电极B吸附O2,电解质溶液为氢氧化钠溶液时,该装置(填“能”或“不能”)形成原电池,若不能,请说明理由,若能,请写出负极电极反应式