甲、乙、丙、丁是由H+、Na+、Al3+、Ba2+、OH—、Cl—、HCO3—离子中的两种组成,可以发生如图转化,下列说法不正确的是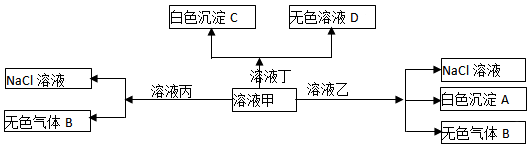
| A.在甲中滴加丁可能发生反应:HCO3—+ Ba2++OH—= BaCO3↓+ H2O |
| B.溶液丙中还可以大量共存的离子有:I—、NO3—、SO42— |
| C.白色沉淀A可能溶解在溶液D中 |
| D.甲为NaHCO3,乙为 AlCl3 |
从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下图表示了三种金属被人类开发利用的大致年限,之所以有先后,主要取决于
| A.金属的导电性强弱 | B.金属在地壳中的含量多少 |
| C.金属的化合价高低 | D.金属的活动性大小 |
下列说法正确的是
| A.18gH2O在标准状况下的体积是22.4L |
| B.22.4LO2中一定含有6.02×1023个氧分子 |
| C.在标准状况时,20mLNH3与60mLN2所含的分子个数为1︰3 |
| D.将80gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为2moL/L |
如图是产生和收集气体的实验装置,该装置不适合于
| A.用盐酸与CaCO3反应制取CO2 | B.用稀硫酸和锌反应制取H2 |
| C.用NH4Cl和Ca(OH)2反应制取NH3 | D.用H2O2溶液和MnO2反应制取O2 |
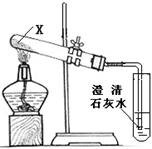
将固体X放在如图所示装置的试管中加热片刻,澄清石灰水变浑浊,X可能是
| A.NaCl | B.CaCl2 | C.Na2CO3 | D.NaHCO3 |
有关Na2CO3和NaHCO3的叙述中正确的是
| A.相同质量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体质量相同 |
| B.Na2CO3比NaHCO3热稳定性强 |
| C.Na2CO3不能与澄清石灰水反应 |
| D.Na2CO3和NaHCO3均可与NaOH溶液反应 |