燃煤能排放大量的CO、CO2、SO2,PM2.5(可入肺颗粒物)污染也跟冬季燃煤密切相关。SO2、CO、CO2也是对环境影响较大的气体,对它们的合理控制、利用是优化我们生存环境的有效途径。
(1)如图所示,利用电化学原理将SO2转化为重要化工原料C

若A为SO2,B为O2,则负极的电极反应式为:________________________;
(2)有一种用CO2生产甲醇燃料的方法:CO2+3H2 CH3OH+H2O
CH3OH+H2O
已知:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-a kJ·mol-1;
CH3OH(g)+H2O(g)△H=-a kJ·mol-1;
2H2(g)+O2(g)=2H2O(g)△H=-b kJ·mol-1;
H2O(g)=H2O(l)△H=-c kJ·mol-1;
CH3OH(g)=CH3OH(l)△H=-d kJ·mol-1,
则表示CH3OH(l)燃烧热的热化学方程式为:____________________________;
(3)光气 (COCl2)是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过Cl2(g)+CO(g)
 COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:
COCl2(g)制备。左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:

① 0~6 min内,反应的平均速率v(Cl2)= ;
② 若保持温度不变,在第7 min 向体系中加入这三种物质各2 mol,则平衡 移动(填“向正反应方向”、“向逆反应方向”或“不”);
③ 若将初始投料浓度变为c(Cl2)=0.7 mol/L、c(CO)=0.5 mol/L、c(COCl2)= mol/L,保持反 应温度不变,则最终达到化学平衡时,Cl2的体积分数与上述第6 min时Cl2的体积分数相同;
④ 随温度升高,该反应平衡常数变化的趋势是 ;(填“增大”、“减小”或“不变”)
⑤比较第8 min反应温度T(8)与第15 min反应温度T(15)的高低:T(8)______________T(15)(填“<”、“>”或“=”)。
酚酞是常用的酸碱指示剂,结构简式为: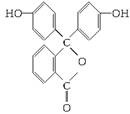
(1)酚酞的分子式为______________________________。
(2)酚酞属于_____________________、________________类衍生物。
(3)酚酞分别在1 mol·L-1 HCl和1 mol·L-1 NaOH溶液中溶解,在_____________中的溶解度大,原因是_________________________________________________________________。
某化工厂的废液经测定得知主要含有乙醇,其中还溶有苯酚(熔点:43 ℃)、乙酸和少量二氯甲烷。现欲从废液中回收它们,根据各物质的熔点和沸点,该工厂设计了以下回收的实验方案。
请完成下列问题:
(1)写出试剂A____________、B____________、C____________的化学式:A____________,B____________,C____________;
(2)写出操作D的名称:D________________;
(3)写出回收物①②和G的组成:①______________,②____________,G____________。
已知:
乙烯酮与活泼的氢化物易发生加成反应,如与HCl的反应如下:
从乙酸出发,可发生下图转化:
完成下列问题:
(1)上面乙酸转化图中,将每种类型反应的个数填入空格,取代反应_____________个,加成反应_____________个,消去反应_____________个。
(2)C的结构简式为_______________________,D的结构简式为____________________。
(3)C的同分异构体甚多,其中含1个—OH和四元环(由3个C、一个O构成)的环酯类化合物有_____________种。
(4)写出A D的化学方程式_______________________________________________。
D的化学方程式_______________________________________________。
分子式为C3H6O3的物质有多种同分异构体,请写出符合下列要求的各种同分异构体的结构简式。说明:①不考虑同一碳原子上连两个羟基;②乙炔、苯等分子中同类原子化学环境相同,丙烷、丁烷等分子中同类原子化学环境有两种。
(1)甲分子中没有甲基,且1 mol甲与足量金属Na反应生成1 mol H2。若甲还能与NaHCO3溶液反应,则甲的结构简式为__________________________;若甲还能发生银镜反应,则甲的结构简式为_________________________。
(2)乙分子中所有同类原子的化学环境相同,且不与金属Na反应,则乙结构简式为:_______。
(3)丙分子中碳与氧分别有两种化学环境,氢的化学环境相同,且丙与金属Na不反应,则丙结构简式为__________________________________________。
硫单质通常是一种淡黄色固体,它的蒸气有橙色、无色、红棕色三种,它们都是硫的单质,但每个分子中硫原子个数不同,可用Sx表示。对这三种蒸气的测定结果如下:
(1)橙色蒸气的密度折算成标准状况后是11.34 g·L-1,则它的化学式为________________。
(2)红棕色蒸气的质量是相同状况下同体积空气的6.62倍,则它的化学式为_____________。
(3)无色蒸气是相同状况下氢气密度的64倍,则它的化学式为______________________。
(4)以上三种蒸气都属于硫单质的____________________。