某小组取一定质量的FeSO4固体,利用下图装置进行实验。

已知:SO2熔点-72℃,沸点-10℃;SO3熔点16.8℃,沸点44.8℃。
| |
实验过程 |
实验现象 |
| ① |
通入一段时间N2,加热 |
A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
| ② |
用带有火星的木条靠近装置D的导管口 |
木条复燃 |
| ③ |
充分反应,停止加热,冷却后,取A中固体,加盐酸 |
固体溶解,溶液呈黄色 |
| ④ |
将③所得溶液滴入D试管中 |
溶液变为浅绿色 |
(1)加热前,先通入一段时间N2的目的是_____________________。
(2)实验③反应的离子方程式是_______________________。
(3)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有_____________气体。依据是______________________。
(4)实验④反应的离子方程式是________________________。
某学生用已知质量y g的表面皿,准确称取w g NaOH固体。他在托盘天平的右盘上放(w+y)g砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边(如右图所示):
(1)下面他的操作应该是______________________,使_________________。
(2)若称取的w g NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制500mLNaOH溶液过程示意图中有错误的是(填操作序号)
某研究性学习小组设想将少量Cl2通入Fe2+和I-的混合溶液,来探究Fe2+和I-的还原性强弱。
【提出假设】
假设1:;
假设2:;
假设3:Fe2+和I-的还原性一样强。
【验证假设】
⑴利用以下装置进行试验,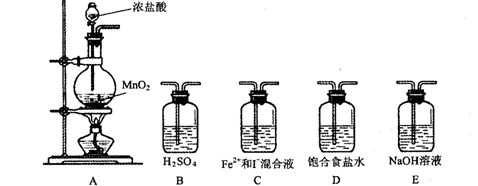
实验必需的装置是:A (按氯气流向的顺序用序号书写)
(按氯气流向的顺序用序号书写) ⑵实验开始后,控制通入少量氯气,通过观察溶液颜色的变化,(能或不能)判断反应的先后顺序。
⑵实验开始后,控制通入少量氯气,通过观察溶液颜色的变化,(能或不能)判断反应的先后顺序。
⑶请在下表中填写实验步骤及预期现象与结论。
| 实验步骤 |
预期现象与结论 |
| 取少量反应的溶液置于A、B两支试管中; 向A试管中滴加; 向B试管中滴加: |
①若 则假设1成立 ②若 则假设2成立 ③若 则假设3成立 |
⑷该实验成功的关键是控制各反应物的用量。该小组称量1.52gFeSO4(M=152g/mol)和1.66gKI(M=166g/mol)固体溶于水中,为了验证上述假设,通入的氯气的体积最多不能超过。(标准状况)
⑸有同学质疑,上述实验只能验证氯气分别与Fe2+和I-反应的速率的大小。并不能证明Fe2+和I-的还原性强弱。于是提出另一验证方案:往KI溶液中滴加溶液,如果能发生反应,就可证明二者的还原性强弱,该反应的离子方程式是。
回答酸碱滴定实验中的下列问题:
(1)下列有关滴定操作的顺序正确的是_______
①检查滴定管是否漏水②用蒸馏水洗涤玻璃仪器③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管④滴定操作⑤装标准溶液和待测液并调整液面(记录初始读数)⑥取一定体积的待测液于锥形瓶中,并滴加指示剂
A.①③②④⑤⑥ B.①②③⑤⑥④ C.②③①④⑤⑥ D.④⑤①②③⑥
(2)下图Ⅰ表示10 mL量筒中液面的位置,A与B、B与C刻度间相差1 mL,如果刻度A为4,量筒中液体的体积是__________mL。
(3)下图Ⅱ表示25.00 mL滴定管中 液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)_
液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)_ _________。
_________。
A.a mL B.(25—a) mL C.大于a mL D.大于(25—a)mL
(4)上图Ⅲ为用一标准浓度NaOH溶液滴定20.00 mL未知浓度的盐酸时的滴定曲线。则两种溶液的物质的量浓度分别是:c(HCl)=________,c(NaOH)=_______________。
(5)滴定过程中,下列操作中会使测定结果偏低的有____________
A.酸式滴定管未润洗 B.锥形瓶内有少量水
C.滴定前,滴定管尖嘴部分有气泡, 滴定后气泡消失
滴定后气泡消失
D.滴定前仰视滴定管读数,滴定后平视刻度读数
实验室用下列方法测定某水样中O2的含量。
(1)用如右图所示装置,使水中溶解的O2,在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为。
实验步骤:
①打开止水夹a 和b,从A 处向装置内鼓入过量N2,此操作的目的是。
②用注射器抽取20.00 mL 某水样从A 处注入锥形瓶。
③再分别从A 处注入含m mol NaOH的溶液及过量的MnSO4 溶液。
④关闭止水夹a、b,将锥形瓶中溶液充分振荡;
(2)用I-将生成的MnO(OH)2再还原为Mn2+,反应的离子方程式为:
MnO(OH)2+2I-+4H+==Mn2++I2+3H2O。
实验步骤:
⑤打开止水夹a、b,分别从A 处注入足量NaI溶液及含n mol H2SO4硫酸溶液。
⑥重复④的操作。
(3)用Na2S2O3标准溶液滴定步骤(2)中生成的I2,反应方程式为:I2+2Na2S2O3==2NaI+Na2S4O6。
实验步骤:
⑦取下锥形瓶,向其中加入2~3滴作指示剂。
⑧用0.005 mol · L-1Na2S2O3滴定至终点。
(4)计算。滴定过程中,滴定前后滴定管中的液面读数如右图所示。
⑨经计算,此水样中氧(O2)的含量为(单位:mg·L-1)。
⑩本实验中所加NaOH溶液和H2SO4溶液中m和n应有一定量的关系,即应加适量的H2SO4使溶液呈(填“酸性”、“碱性”或“接近中性”),其原因是。
用98%的浓H2SO4(ρ=1.84g/cm3)配制240mL0.5mol/L的稀H2SO4,请按要求填空:
(1)所用浓H2SO4的物质的量浓度为 ,配制时所需浓硫酸的体积为mL。(均保留一位小数)
(2)实验中需要用到的定量仪器有。
(3)若实验中出现下列现象对所配溶液的浓度有什么影响?(填“偏高”、“偏低”或“无影响”)
①浓硫酸溶解后未冷至室温即进行转移、定容。()
②定容时俯视刻度线。()
(4)若定容时液面高于刻度线应采取的措施是。
(5)若实验操作全部无误,最后所得的溶液应存放在试剂瓶中,并贴上标签,请你帮助把标签上的内容写一下(如右图)。