某温度下,密闭容器中,发生如下可逆反应:2E(g) F(g)+xG(g);
F(g)+xG(g);
ΔH<0。若起始时E浓度为a mol/L,F、G浓度均为0,达平衡时E浓度为0.5a mol/L;若E的起始浓度改为2a mol/L,F、G浓度仍为0,当达到新的平衡时,下列说法正确的是
| A.若x=l,容器体积保持不变,新平衡下E的体积分数为50% |
| B.升高温度时,正反应速率加快、逆反应速率减慢 |
| C.若x=2,容器体积保持不变,新平衡下F的平衡浓度为0.5a mol·L-1 |
| D.若x=2,容器压强保持不变,新平衡下E的物质的量为a mol |
在下列给定的溶液中,一定能大量共存的离子组是()
| A.过量Al与NaOH溶液反应所得溶液中:K+、Cl-、Al3+、SO42- |
| B.常温下,OH-的浓度为10-11mol/L的溶液中:Na+、I-、NH4+、NO3- |
C.常温下,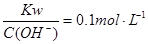 的溶液中:K+、NH4+、Cl-、SO42- 的溶液中:K+、NH4+、Cl-、SO42- |
| D.与Al反应产生H2的溶液中:K+、Na+、I-、NO3- |
有一支50mL酸式滴定管其中盛有溶液,液面恰好在10mL刻度处,现把管内溶液全部流下排出,用量筒承接,该溶液的体积应为()
| A.10mL | B.大于40mL | C.40mL | D.小于40mL |
下列说法正确的是()
| A.将pH=3的醋酸稀释后,溶液中所有离子的浓度均降低 |
| B.在纯水中加入少量NaOH或醋酸钠均可抑制水的电离 |
| C.常温下,将pH=3的盐酸和pH=11的氨水等体积混合,溶液的pH>7 |
| D.用标准NaOH溶液滴定醋酸至刚好完全反应时,溶液中C(Na+)=C(CH3COO-) |
单斜硫和正交硫是硫的两种同素异形体()
已知:①S(单斜,S)+O2(g)===SO2(g),△H=-297.16 kJ·mol-1
②S(正交,S)+O2(g)===SO2(g),△H2=-296.83 kJ·mol-1
③S(单斜,S)===S(正交,s),△H3
下列说法正确的是()
| A.△H3="0.33" kJ·mol-1 | B.单斜硫转化为正交硫的反应是吸热反应 |
| C.△H3<0,正交硫比单斜硫稳定 | D.△H3>0,单斜硫比正交硫稳定 |
在配置Fe2(SO4)3溶液时,为了防止水解,常常往溶液中加入少量的:()
| A.NaOH | B.H2SO4 | C.KCl | D.CH3COOH |