下列离子方程式与所述事实相符且正确的是
| A.漂白粉溶液在空气中失效:ClO-+ CO2 + H2O ="===" HClO + HCO3- |
| B.用浓盐酸与MnO2反应制取少量氯气: MnO2+2H++2Cl- 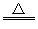 Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| C.向Na[Al(OH)4]溶液中通入过量CO2制Al(OH)3∶ [Al(OH)4]-+ CO2==== Al(OH)3↓ + HCO3- |
| D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4: |
3ClO-+2Fe(OH)3====2FeO42-+3Cl-+H2O+4H+
在某温度下,H2和I2各0.10mol的气态混合物充入10L的密闭容器中,发生反应:H2(g)+I2(g)  2HI(g),充分反应后达到平衡,测得c(H2)="0.008" mol•L-1,则该反应的平衡常数为
2HI(g),充分反应后达到平衡,测得c(H2)="0.008" mol•L-1,则该反应的平衡常数为
| A.40 | B.62.5 | C.0.25 | D.4 |
在恒温恒容的密闭容器中,对于可逆反应A(g)+B(g)  2C(g),可以判断达到化学平衡状态的是
2C(g),可以判断达到化学平衡状态的是
| A.体系压强不变 | B.单位时间消耗n molA,同时生成2nmolC |
| C.A的转化率不变 | D.容器内气体密度不变 |
把下列四种 X 溶液分别加入四个盛有 10mL2 mol•L-1盐酸的烧杯中,均匀加水稀释到50mL。此时X 和盐酸缓缓地进行反应。其中反应速率最大的是
| A.20mL 3 mol•L-1的 X 溶液 | B.20mL 2 mol•L-1的 X 溶液 |
C. 10mL 4 mol•L-1的 X 溶液 10mL 4 mol•L-1的 X 溶液 |
D.l0mL 2 mol•L-1的 X 溶液 |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间的变化曲线如图,下列表述中正确的是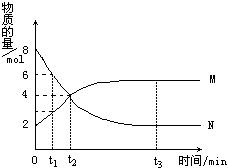
A.反应的化学方程式为:2M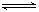 N N |
B.t2时,正逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 | D.t1时,N的浓度是M浓度的2倍 |
下图是关于反应A2(g)+3B2(g)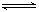 2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是
2C(g)(正反应为放热反应)的平衡移动图象,影响平衡移动的原因可能是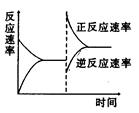
| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时减小生成物浓度 |
| D.增大反应物浓度,同时使用催化剂 |