现在要分离下列物质,将分离方法的字母序号填在横线上。
| A.萃取 | B.加热分解 |
| C.结晶 | D.分液 |
E.蒸馏 F.过滤
(1)要除去NaCl溶液中的泥沙__________________
(2)用CCl4提取溴水中的溴单质_________________
(3)分离互溶的乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃)__________________
(4)分离汽油和水_________________
(5)从含有少量的NaCl的KNO3溶液中提取KNO3_________________
(6)生石灰中含有石灰石的杂质_________________
实验室用4 mol SO2与2 mol O2在一定条件下进行下列反应:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.64 kJ·mol-1,当放出314.624 kJ热量时,SO2的转化率为________。
2SO3(g) ΔH=-196.64 kJ·mol-1,当放出314.624 kJ热量时,SO2的转化率为________。
I、在 K2Cr2O7+14HCl═2KCl+2CrCl3+3Cl2↑+7H2O反应中.
(1) 元素被氧化, 是氧化剂;
(2)在该反应中若有0.5mol K2Cr2O7被还原,则被氧化的HCl的物质的量为 mol.
Ⅱ、将铁粉、铜粉、氯化铁溶液、氯化亚铁溶液和氯化铜溶液,混合于容积合适的烧杯内,充分反应后,试填写下列空白.
(1)若铁粉有剩余,则溶液中不可能有的离子是 (从Fe3+、Cu2+、Fe2+中选填).
(2)若溶液中氯化铁和氯化铜都有剩余,则不可能有的金属单质是 (从Fe、Cu中选填).
Ⅰ、处于下列状态的物质中:①NaCl ②CO2 ③NH3·H2O④Cu ⑤HCl ⑥NaOH ⑦酒精 ⑧H2O ⑨NaCl溶液 ⑩NH3
(1)属于强电解质的是 (填序号,下同) ;
(2)属于弱电解质的是 ;
(3)属于非电解质的是 ;
Ⅱ、写出下列反应的离子方程式
(1)向澄清石灰水中加盐酸 ;
(2)用石灰石与盐酸反应制取二氧化碳 ;
(3)氢氧化钠溶液与氯化铵溶液混合后加热 ;
(1)对于可逆反应,升高温度,化学平衡向 热反应方向移动。
(2)对于有气体参加的可逆反应,增大压强,化学平衡向气体体积 (增大或小) 的方向移动。
(3)使用催化剂,能同等程度的改变正逆化学反应速率,化学平衡
(4)氢气的燃烧热为285.8千焦,其热化学方程式为:
(5)甲溶液的pH是4,乙溶液的pH是5,甲溶液与乙溶液的c(H+))之比:
在密闭容器中进行反应①Fe(s)+CO2(g)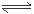 FeO(s)+CO(g)ΔH1=akJ·mol一1
FeO(s)+CO(g)ΔH1=akJ·mol一1
反应②2CO(g)+O2(g)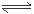 2CO2(g)△H2="b" kJ·mol-1
2CO2(g)△H2="b" kJ·mol-1
反应③2Fe(s)+O2(g)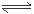 2FeO(s) △H3
2FeO(s) △H3
(1) △H3= (用含a、b的代数式表示)。
(2)反应①的化学平衡常数表达式K= ,已知500℃时反应①的平衡常数K=1.0,在此温度下2 L密闭容器中进行反应①,Fe和CO2的起始量均为2.0 mol,达到平衡时CO2的转化率为 ,CO的平衡浓度为 。
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是CO2浓度的两倍,则a 0(填“>”、“<”或“=”)。为了加快化学反应速率且使体系中CO的物质的量增加,其他条件不变时,可以采取的措施有 (填序号)。
| A.缩小容器的体积 | B.再通入CO2 |
| C.升高温度 | D.使用合适的催化剂 |
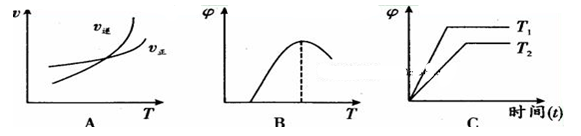
(4)下列图像符合反应①的是 (填序号)(图中V是速率、φ为混合物中CO含量,T为温度)。