实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对就还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中逐滴加入5mol/L NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列说法不正确的是
| A.稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵 |
| B.c点对应NaOH溶液的体积为48 mL |
| C.b点与a点的差值为0.05 mol |
| D.样品中铝粉和铁粉的物质的量之比为5:3 |
下列有关仪器的使用方法或实验操作正确的是( )
| A.洗净的锥形瓶和容量瓶可以放进烘箱中烘干 |
| B.酸式滴定管装标准液前,必须先用该溶液润洗 |
| C.酸碱滴定实验中,用待测溶液润洗锥形瓶以减小实验误差 |
| D.用容量瓶配溶液时,若加水超过刻度线,立即用滴定管吸出多余液体。 |
用NA表示阿伏加德罗常数的值。下列说法不正确的是( )
| A.在一定条件下,催化分解80 g SO3所得混合气体中氧原子数为3NA |
| B.一定条件下,铁与水蒸气反应生成8.96 L(已折合成标准状况)H2时,转移的电子数为0.8NA |
| C.将100 mL 1 mol/L AlCl3与100 mL 3 mol/L NaCl溶液混合后,Cl-的个数为0.6NA |
| D.含有非极性键的数目为NA的Na2O2与水充分反应产生标准状况下22.4 L O2 |
把足量的铁粉投入到稀盐酸和氯化铜的混合溶液中,充分反应后,残余固体的质量与原来加入的铁粉质量相等,则原溶液中H+和Cl-的物质的量之比为( )
| A.1∶4 | B.1∶7 | C.1∶8 | D.2∶5 |
下列关于物质的量浓度表述正确的是( )
A.0.3 mol·L-1的Na2SO4溶液中含有Na+和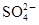 的总物质的量为0.9 mol 的总物质的量为0.9 mol |
| B.当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol·L-1,当22.4 L氨气溶于水制得1 L氨水时,其浓度才是1 mol·L-1 |
C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和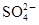 的物质的量相等,则K+和Cl-的物质的量浓度一定相同 的物质的量相等,则K+和Cl-的物质的量浓度一定相同 |
| D.10 ℃时,100 mL 0.35 mol·L-1的KCl饱和溶液蒸发掉5 g水,冷却到10 ℃时,其体积小于100 mL,它的物质的量浓度仍为0.35 mol·L-1 |
如图中的两条线分别代表的是:1 g C3H6和1 g M气体在相同容积的容器中,测得容器中的压强和温度的关系,试根据图形判断M气体可能是( )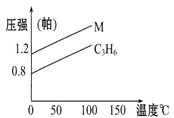
| A.C3H8 | B.C2H4 |
| C.H2S | D.N2O4 |