已知2H2(g)+O2(g)=2H2O(l);ΔH=-571.6kJ/mol,CO(g)+O2(g)=CO2(g);ΔH=-282.9kJ/mol某H2和CO的混合气体完全燃烧时放出113.74kJ热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为
| A.1∶1 | B.1∶2 | C.2∶1 | D.2∶3 |
厨房中的化学知识很多,下面是有关厨房中的常见操作或者常见现象,其中不属于氧化还原反应的是( )
| A.烧菜用过的铁锅,经放置常出现红棕色斑迹 |
| B.用煤气灶燃烧沼气(主要成分为甲烷:CH4)为炒菜提供热量 |
| C.牛奶久置变质腐败 |
| D.用醋酸除去水垢[主要成分是CaCO3、Mg (OH)2] |
国际互联网上报道:“目前世界上有近20亿人患有缺铁性贫血”,我国政府现已启动“酱油补铁工程”,这里的铁指的是( )
| A.铁元素 | B.铁单质 | C.四氧化三铁 | D.硫酸铁 |
在一密闭容器中有如下反应:aX(g)+bY(g) nW(g) ΔH,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
nW(g) ΔH,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图: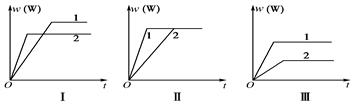
其中,w(W)表示W在反应混合物中的体积分数,t表示反应时间。下列分析正确的是( )
| A.图Ⅰ可能是不同压强对反应的影响,且p1>p2,a+b<n |
| B.图Ⅱ可能是不同压强对反应的影响,且p1>p2,n<a+b |
| C.图Ⅱ可能是在同温同压下不同催化剂对反应的影响,且Ⅰ使用的催化剂效果好 |
| D.图Ⅲ可能是不同温度对反应的影响,且T1>T2,ΔH<0 |
可逆反应mA(g) nB(g)+pC(s) ΔH=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( )
nB(g)+pC(s) ΔH=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( )
| A.m>n,Q>0 | B.m>n+p,Q>0 |
| C.m>n,Q<0 | D.m<n+p,Q<0 |
在不同条件下分别测得反应2SO2+O2 2SO3的化学反应速率,其中表示该反应进行的最快的是( )
2SO3的化学反应速率,其中表示该反应进行的最快的是( )
| A.v(SO2)=4 mol/(L·min) | B.v(O2)=3 mol/(L·min) |
| C.v(SO2)=0.1 mol/(L·s) | D.v(O2)=0.1 mol/(L·s) |