对下列实验现象的原因分析不正确的一项是
| 选项 |
实验现象 |
原因分析 |
| A |
浓硫化钠溶液有臭味 |
硫离子水解生成硫化氢,硫化氢具有臭味 |
| B |
新制氯水中滴加石蕊试液,溶液先变红,后褪色 |
氯气与水反应生成HCl、HClO,HCl显强酸性,使石蕊变红,HClO具有强氧化性,使其褪色 |
| C |
SO2通入溴水中,溴水褪色 |
SO2具有漂白性,使其褪色 |
| D |
向湿润蔗糖中加入浓硫酸,固体迅速变黑,后体积急剧膨胀 |
在浓硫酸脱水作用下,蔗糖被炭化,炭与浓硫酸反应生成了CO2、SO2 |
雾霾,是雾和霾的统称。空气中的灰尘、硫酸、硝酸等颗粒物组成的气溶胶系统造成视觉障碍的叫霾。当水汽凝结加剧、空气湿度增大时,霾就会转化为雾。二氧化硫、氮氧化物和可吸入颗粒物这三项是雾霾主要组成。以下说法不正确的是()
| A.雾霾天,汽车车灯照出通路的现象属于丁达尔现象 |
| B.冬天烧煤时可在煤中加入生石灰减少二氧化硫的排放 |
| C.防霉霾口罩的原理与过滤、渗折类似,防雾霉效果好的口罩往往呼吸阻力较大 |
| D.PM 2.5是直径小于等于2.5微米的污染物颗粒,完全属于胶体粒子的直径范围 |
某同学用下列装置验证一些物质的性质。下列说法错误的是()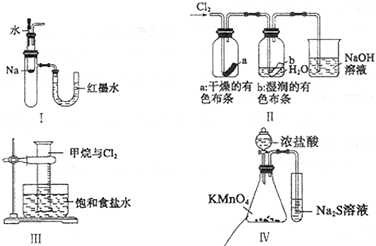
| A.Ⅰ图中:将胶头滴管中的水滴入到金属钠中,能看到U型管右侧红墨水上升 |
| B.Ⅱ图中:观察到湿润的有色布条能褪色,待尾气全部被碱吸收后,将稀硫酸滴入烧杯中,至溶液显酸性,可能看到有黄绿色气体生成 |
| C.Ⅲ图中:观察到量筒内黄绿色逐渐消失,量筒内壁有油状物质生成。该现象是由于甲烷与氯气在光照条件下发生了加成反应 |
D.Ⅳ图中,可以比较 、 、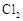 和S氧化性的相对强弱 和S氧化性的相对强弱 |
关于离子浓度的关系,下列说法错误的是()
A.等浓度的 、 、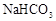 混合溶液中: 混合溶液中:  |
B.新制氯水中: |
C.室温下,向0.01  溶液中滴加 溶液中滴加 溶液至中性: 溶液至中性: |
D.物质的量浓度均为 的 的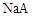 和 和 混合溶液中,离子浓度可能的关系为: 混合溶液中,离子浓度可能的关系为: |

化学平衡常数(K)、电离常数(Ka、Kb)、溶度积常数(Ksp)等常数是表示、判断物质性质的重要常数,下列关于这些常数的说法中,正确的是()
| A.化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关 |
| B.Ka(HCN)<Ka(CH3COOH)说明相同物质的量浓度时,氢氰酸的酸性比醋酸强 |
| C.向氯化钡溶液中加入同浓度的碳酸钠和硫酸钠溶液,先产生BaSO4沉淀,则Ksp(BaSO4)>Ksp(BaCO3) |
| D.当温度升高时,弱酸、弱碱的电离常数(Ka、Kb)变大 |
E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:xM(g) Mx(g),反应物和生成物的物质的量随时间的变化关系如图。下列说法正确的是()
Mx(g),反应物和生成物的物质的量随时间的变化关系如图。下列说法正确的是()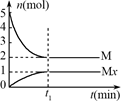
| A.M的沸点比同主族下一周期元素的气态氢化物沸点低 |
B.该反应的百分比学方程式是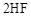  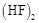 |
| C.平衡时混合气体的平均摩尔质量是33.3 |
D.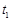 时刻,保持温度不变,再充入1 molM,重新达到平衡时, 时刻,保持温度不变,再充入1 molM,重新达到平衡时,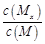 将增大 将增大 |