合成氨工业为人类解决粮食问题做出了巨大贡献.一定条件下,在密闭容器中进行合成氨反应:N2(g)+3H2(g)⇌2NH3(g),当正、逆反应速率相等且不等于零时,下列说法不正确的是
| A.N2、H2完全转化为NH3 |
| B.N2、H2、NH3在容器中共存 |
| C.反应已达到化学平衡状态 |
| D.N2、H2、NH3的浓度不再改变 |
取未知浓度的硫酸、盐酸和醋酸各25.00mL,分別用0.10mol·L-1的NaOH溶液或0.10mol·L-1的稀氨水滴定得下图。下列说法正确的是
| A.由图可知曲线c为NaOH滴定硫酸 |
| B.由图可知硫酸的物质的量浓度大于盐酸的物质的量浓度 |
| C.曲线b、c的滴定实验可用酚酞做指示剂 |
| D.由图可知滴定前醋酸电离度约为1.67﹪ |
一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合下图的是
A.CO2(g)+2NH3(g)  CO(NH2)2(s)+H2O(g);ΔH<0 CO(NH2)2(s)+H2O(g);ΔH<0 |
B.CO2(g)+H2(g)  CO(g)+H2O(g);ΔH>0 CO(g)+H2O(g);ΔH>0 |
C.CH3CH2OH(g)  CH2==CH2(g)+H2O(g);ΔH>0 CH2==CH2(g)+H2O(g);ΔH>0 |
D.2C6H5CH2CH3(g)+O2(g)  2C6H5CH=CH2(g)+2H2O(g);ΔH<0 2C6H5CH=CH2(g)+2H2O(g);ΔH<0 |
某同学组装了如图所示的电化学装置,其中电极Ⅰ为Al,其它均为Cu,下列说法正确的是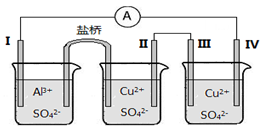
| A.装Al2(SO4)3溶液的烧杯是原电池,其余两个为电解(电镀)池 |
| B.盐桥中电子从右侧流向左侧 |
| C.电极Ⅱ逐渐溶解 |
| D.电极IV的电极反应:Cu2+ + 2e- = Cu |
下列说法正确的是
| A.实验中需用0.20 mol·L-1的NaOH溶液950mL,配制时应称取NaOH的质量8.0g |
| B.升高NH4Cl溶液温度,其水的离子积常数和pH均增大 |
| C.水比硫化氢稳定的原因是水分子间存在氢键 |
| D.在pH等于2的醋酸溶液中加入少量0.01 mol·L-1的稀盐酸,溶液的pH会变小 |
已知下列四个反应的能量与反应进程变化关系如图:
①H2SO4(aq) + 2NaOH(aq) = Na2SO4(aq) + 2H2O(l)
②CH3CH2OH(g) + 3O2(g) = 2CO2 (g)+ 3H2O(g)
③N2(g) + 3H2(g) = 2NH3(g)
④Ba(OH)2(s) + 2NH4Cl (s)= BaCl2(s) + 2NH3(g)+ 2H2O(l)
则反应②对应能量进程图可能是
| A.图一 | B.图二 | C.图三 | D.图四 |