目前下列工艺过程没有直接使用离子交换技术的是
| A.硬水的软化 | B.电解饱和食盐水制造NaOH |
| C.电渗析淡化海水 | D.海水中提取金属镁 |
观察下列模型并结合有关信息,判断有关说法不正确的是()
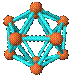
| B12结构单元 |
SF6分子 |
S8分子 |
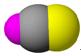
HCN |
|||||
| 结构模型示意图 |
 |
 |
 |
 |
||||
| 备注 |
熔点1873K |
/ |
易溶于CS2 |
/
|
下列说法中正确的是()
| A.氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物 |
| B.碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力 |
| C.氧气和臭氧间的相互转化属于氧化还原反应 |
| D.有机化合物CH3—CH2—NO2和H2N—CH2—COOH是同分异构体 |
下列说法中正确的是()
| A.晶体中一定存在化学键 |
| B.非金属元素之间形成的化学键不一定是共价键 |
| C.含有共价键的化合物一定是共价化合物 |
D.正四面体分子中键角一定是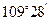 |
下列有关比较中,大小顺序排列错误的是()
| A.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| B.物质的熔点:石英>食盐>冰>汞 |
| C.晶体的晶格能CaO>NaCl>CsCl |
| D.热稳定性:PH3>H2S>HBr>NH3 |
图表资料可以为我们提供很多信息,下列关于图表提供的资料或应用的说法中,不正确的是() NvQ"xKN
| A.利用元素周期表可以预测新元素的原子结构和性质MRI7 ? |
| B.根据酸、碱、盐的溶解性表,可判断酸、碱、盐的溶解度 hk]7>}eYn? |
| C.根据电负性表,可判定2种元素形成的化学键是离子键还是共价键 d:="}5JGIQ" |
| D.核磁共振氢谱可以用来测定分子中H原子种类和个数比 |