【化学——选修3:物质结构与性质】
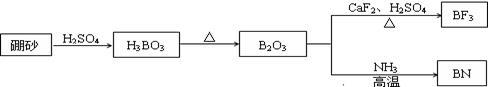
氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
请回答下列问题:
(1)由B3O3制备BF3、BN的化学方程式依次是_____________、_____________;
(2)基态B原子的电子排布式为____________;B和N相比,电负性较大的是___________,BN中B元素的化合价为______________;
(3)在BF3分子中,F—B—F的键角是____________,B原子的杂化轨道类型为____________,BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为_____________;
(4)在与石墨结构相似的六方氮化硼晶体中,层层内B原子与N原子之间的化学键为___________,层间作用力为___________;
(5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有_________________个氮原子、______________个硼原子,立方氮化硼的密度是_________________g.cm-3(只要求列算式,不必计算出数值。阿伏伽德罗常数为NA)。
由熔盐电解法获得的粗铝含一定量的金属钠和氢气,这些杂质可采用吹气精炼法除去,产生的尾气经处理后可用于钢材镀铝。工艺流程如下:
(注:NaCl熔点为801 ℃;AlCl3在181 ℃升华)
(1)精炼前,需清除坩埚表面的氧化铁和石英砂,防止精炼时它们分别与铝发生置换反应产生新的杂质,相关的化学方程式为:
①____________
②____________。
(2)将Cl2连续通入坩埚中的粗铝熔体,杂质随气泡上浮除去。气泡的主要成分除Cl2外还含有_________;固态杂质粘附于气泡上,在熔体表面形成浮渣,浮渣中肯定存在__________。
(3)在用废碱液处理气体A的过程中,所发生反应的离子方程式为:________________。
(4)镀铝电解池中,金属铝为________极。熔融盐电镀液中铝元素和氯元素主要以AlCl4-和Al2Cl7-形式存在,铝电极的主要电极反应式为___________。
(5)钢材镀铝后,表面形成的致密氧化铝膜能防止钢材腐蚀,其原因是______________。
现有A、B、C、D、E、F六种化合物,已知它们的阳离子分别是K+、Ag+、Ca2+、Ba2+、Fe2+、Al3+,阴离子分别是Cl-、OH-、CH3COO-、NO3-、SO42-、CO32-,将它们分别配成0.1 mol/L的溶液,进行如下实验:
①测得溶液A、C、E呈碱性,且碱性为A>E>C;
②向B溶液中滴加稀氨水,先出现沉淀,继续滴加氨水,沉淀消失;
③向D溶液中滴加Ba(NO3)2溶液,无明显现象;
④向F溶液中滴加氨水,生成白色絮状沉淀,沉淀迅速变成灰绿色,最后变成红褐色。
根据上述实验现象,回答下列问题:
(1)实验②中反应现象所涉及的离子方程式是_____ ________。
(2)E溶液中溶质的名称是___________,判断依据是__________。
(3)写出下列四种化合物的化学式:
A:_______________ C:_____________ D:_______________ F:_______________
化合物Ⅰ(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。Ⅰ可以用E 和H在一定条件下合成: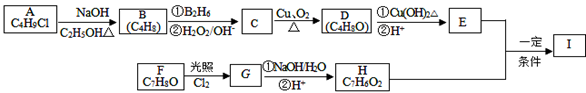
已知:①A的核磁共振氢谱表明其只有一种化学环境的氢;
②RCH=CH2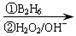 RCH2CH2OH
RCH2CH2OH
③化合物F苯环上的一氯代物只有两种;
④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
(1)A的化学名称为 ;
(2)D的结构简式为 ;
(3)I的结构简式为 ;
(4)写出下列反应的类型:A→B: ;C→D: _____________
(5)F生成G的化学方程式为:_______________;
(6)I的同系物J比I相对分子质量小14,J能同时满足如下条件:①苯环上只有两个取代基,②能发生银镜反应,③能和饱和NaHCO3溶液反应放出CO2;符合上述条件的同分异构体共有 种(不考虑立体异构)。若J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式_______________。
某芳香族化合物A式量小于150,氢氧质量比为1∶8,完全燃烧后只生成CO2和H2O。取等质量的A分别与足量NaHCO3和Na反应,生成的气体在同温同压下的体积比为1∶1。工业常用A来合成药物B及医药中间体G,流程如下: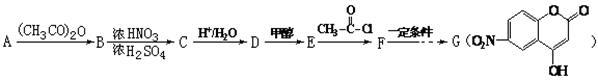
已知:①
②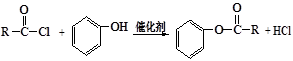
(1)写出A含有的官能团的名称 ,D的结构简式 。
(2)D生成E的反应类型是 。
(3)写出F与过量NaOH共热时反应的化学方程式: 。
(4)A自身之间也能发生缩聚反应,写出该高分子聚合物的化学式 。
(5)B有多种同分异构体,写出符合下列条件的一种物质的结构简式 。
①只有一种官能团②苯环上的一氯取代物只有二种
③能发生银镜反应④核磁共振谱共有四组峰,峰的面积比为3∶2∶2∶1
(6)下列有关说法正确的是 。
| A.可由A经一步反应获得D; |
B. 与G互为同分异构体 与G互为同分异构体 |
| C.G易水解,可用FeCl3溶液检验是否发生水解 |
| D.1 molG一定能和5mol氢气反应 |
已知有机物A~I之间的转化关系如下图所示:
注;O表示有机物发生了氧化反应
已知:①A与D、B与E、I与F互为同分异构体
②将新制Cu(OH)2悬浊液分别加入到有机物I、F中,加热,I无明显现象,F反应并生成砖红色物质
③C的实验式与乙炔相同,且相对分子质量为104
④E的一种同分异构体与FeCl3能发生显色反应
根据以上信息,回答下列问题:
(1)H、 F中含有的含氧官能团名称分别为 、 。
(2)反应①~⑨中属于消去反应的是______________________。
(3)I的结构简式为____________________。
(4)写出H在酸性条件下水解的化学方程式____________________。
(5)写出F与银氨溶液反应的化学方程式 _________________。
(6)符合以下条件的G的同分异构体有________种;
①属于芳香族化合物 ②能与NaOH溶液反应 ③能发生银镜反应
其中苯环上一元取代物只有2种的结构简式为 。