25℃时,用0.1mol·L-1的CH3COOH溶液滴定20mL0.1mol·L-1的NaOH溶液,当滴加VmLCH3COOH溶液时,混合溶液的pH=7。已知CH3COOH的电离平衡常数为Ka,忽略混合时溶液体积的变化,下列关系式正确的是
A.Ka= |
B.V= |
C.Ka=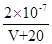 |
D.Ka= |
对下列实验现象的解释不正确的是( )
| 选项 |
实验现象 |
解释 |
| A |
C12使鲜艳的红色花瓣褪色 |
Cl2具有强还原性 |
| B |
NH3与HCl气体接触时有白烟产生 |
NH3与HCl反应生成固体小颗粒 |
| C |
新切开的Na表面在空气中很快变暗 |
Na容易与空气中的氧气等反应 |
| D |
氯化铝溶液中滴入过量的氢氧化钠溶液,白色沉淀溶解 |
氢氧化铝具有两性 |
在一定条件下,将等体积的NO和 NO2充入试管,并将试管倒立于水槽中,充分反应后剩余气体的体积缩小为原体积的()
| A.1/2 | B.1/3 | C.3/8 | D.2/3 |
下列各组物质的稀溶液相互反应,把前者逐滴滴入后者与把后者逐滴滴入前者,所产生的现象相同的是()
| A.AlCl3和NaOH | B.Na2CO3和HCl |
| C.NaAlO2和HCl | D.NaCl和AgNO3 |
为了除去FeSO4溶液中少量的Fe2(SO4)3和CuSO4杂质,可选用的试剂是()
| A.Fe | B.氨水 | C.NaOH | D.氯水 |
下列可用于检验实验室久置的FeSO4溶液是否含有Fe3+的试 剂是
剂是
| A.石蕊试液 | B.酚酞试液 | C.新制氯水 | D.KSCN溶液 |