书写下列反应的热化学方程式
(1)1molN2(g)与适量O2(g)反应生成NO (g),需吸收68kJ的热量
(2)1 L 1 mol/L 稀盐酸跟 1 L 1 mol/L NaOH溶液起中和反应放出57 .3 kJ热量
(3)在25℃、1.01×105Pa时,16g S粉在足量的氧气中充分燃烧生成二氧化硫气体,放出148.5KJ的热量,则S的燃烧热的热化学方程式为
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且不会造成二次污染。已知高铁酸盐热稳定性差,工业上用湿法制备高铁酸钾的基本流程如下图所示:
(1)上述氧化过程中,发生反应的离子方程式是:,控制反应温度30℃以下的原因是:。
(2)结晶过程中加入浓KOH溶液的作用是:。
(3)根据图1、图2回答:为了获取更多的高铁酸钾,铁盐的质量分数应控制在附近、反应时间应控制在。
利用天然气合成氨的工艺流程示意图如下: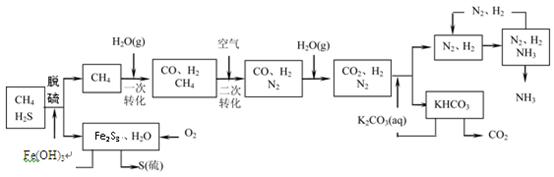
依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是。
(2)图中CH4的第一次转化过程中的化学方程式是。
(3)整个流程有三处循环,一是K2CO3(aq)循环,二是N2和H2循环,三是(填化学式)循环。
(4)K2CO3(aq)和 CO2反应在加压下进行,加压的理论依据是(多选扣分)。
a.熵增原理b.勒夏特列原理c.酸碱中和原理
A、B、C、 D四种溶液分别是NaOH溶液、氨水、 CH3COOH溶液、盐酸中的一种。常温下:
①浓度均为0.1mol·L-1的A和C溶液,pH:A<C<7;
②将1 L pH=3的A溶液分别与0.001mol·L-1xL B溶液、0.001mol·L-1yL D溶液充分反应至中性,x、y大小关系为: y<x;
回答下列问题:
(1)D是(填化学式)溶液;
(2)②中1LpH=3的A溶液与0.001mol·L-1 xL B溶液充分反应至中性,所 得溶液中各种离子的物质的量浓度由大到小的顺序为。
得溶液中各种离子的物质的量浓度由大到小的顺序为。
(3)常温下,等体积且等物质的量浓度的C溶液和D溶液充分混合后所得溶液的pH
7(填“>”、“<”或“=”),用离子方程式解释其原因。
(4)向pH相同且等体积的两份溶液A和C中,分别投入质量不同的锌粉反应,若放出氢气的质量相同,则下列说法正确的是(填写序号)。
①开始反应时的速率A>C②反应所需要的时间C>A
③参加反应的锌粉物质的量A="C" ④A溶液里有锌粉剩余
硫酸是工业生产中最为重要的产品之一。在催化反应室里进行的反应为:
2SO2(g)+O2(g) 2SO3(g)ΔH=" –196.6" kJ·mol-1
2SO3(g)ΔH=" –196.6" kJ·mol-1
(1)该反应发生的条件通常是400~500℃、和。
(2)SO3在(填设备名称)中用(填试剂名称)吸收。
(3)研究SO2 、NO2、CO等大气污染气体的处理具有重要意义。
已知: 2NO(g)+O2(g) 2NO2(g)ΔH=" –113.0" kJ·mol-1
2NO2(g)ΔH=" –113.0" kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=kJ·mol-1。
SO3(g)+NO(g)的ΔH=kJ·mol-1。
一定条件下,将NO2与SO2以物质的量之比1:2置于恒容密闭容器中发生上述反应,下列能说明反应达到平衡状态的是。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2的物质的量之比为1:6,则平衡常数K=。
有机物A的分子中碳氢原子数之比为1:2。它不与碳酸钠反应,相同物质的量的A与氢气的质量比为37:1 。0.37g A与足量的银氨溶液反应可析出1.08g Ag.A在一定条件下与氢气反应生成B,1mol B 与足量金属钠反应可产生22.4LH2(标准状况下),B不与碳酸钠反应.写出所有符合条件的A、B的结构简式。
AB