能源短缺是全球面临的问题,用CO2来生产燃料甲醇的反应原理为
CO2(g)+3H2(g)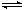 CH3OH(g)+H2O(g) 已知某些化学键的键能数据如表所示:
CH3OH(g)+H2O(g) 已知某些化学键的键能数据如表所示:
| 化学键 |
C-H |
H-H |
C-O |
C=O |
H-O |
| 键能/kJ·mol-1 |
413.4 |
436.0 |
351.0 |
745.0 |
462.8 |
则该反应的焓变△H为
A.-46.2 kJ· mol-1 B.+46.2 kJ· mol-1
C.-181.6 kJ· mol-1 D.+181.6 kJ· mol-1
某原电池的总反应的离子方程式是:Zn+Cu2+=Zn2++Cu,此反应的原电池正确的是( )
| [ |
正极 |
负极 |
电解质溶液 |
| A |
Cu |
Zn |
HCl |
| B |
Zn |
Cu |
CuSO4 |
| C |
Ag |
Zn |
CuSO4 |
| D |
Cu |
Zn |
ZnCl2 |
对于A2(g) + 3B2(g) 2C(g)+ D(g)反应来说,以下化学反应速率的表示中,反应速率最快的是
2C(g)+ D(g)反应来说,以下化学反应速率的表示中,反应速率最快的是
A.v(A2)=0.4mol/(L•s) B.v(B2)=0.8mol/(L•s)
C.v(C)=0.6mol/(L•s) D.v(D)=0.3mol/(L• s)
下列有关化学反应中能量变化的理解正确的是
| A.凡是伴有能量的变化都是化学变化 |
| B.反应物的总能量高于生成物的总能量时,发生放热反应 |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.单质A转化为单质B是一个吸热过程,可知单质B比单质A稳定 |
测定中和热的实验中,一组完整的实验数据至少需要测温度几次
| A.1次 | B.2次 | C.3次 | D.4次 |
中子数比质子数多1个的原子A,其阳离子An+ 核外有X个电子,则A的质量数为
| A.2(x+n) | B.2(x-n) +1 | C.2(x +n) +1 | D.n+2 |