工业上可利用“甲烷蒸气转化法生产氢气”,反应为:
CH4(g)+H2O(g)  CO(g)+3H2(g)
CO(g)+3H2(g)
已知温度、压强和水碳比[n(H2O)/n(CH4)]对甲烷平衡含量(%)的影响如下图1:
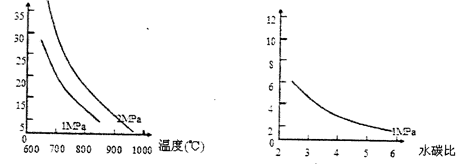
图1 (水碳比为3) 图2 (800℃)
(1)CH4(g)+H2O(g)  CO(g)+3H2(g)。的
CO(g)+3H2(g)。的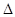 H 0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将 移动(填“向正应方向”、“向逆反应方向”或“不”)。
H 0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将 移动(填“向正应方向”、“向逆反应方向”或“不”)。
(2)温度对该反应的反应速率和平衡移动的影响是 。
(3)其他条件不变,请在图2中画出压强为2MPa时,甲烷平衡含量(%)与水碳比之间关系曲线。(只要求画出大致的变化曲线)
(4)已知:在700℃,1MPa时,1mol CH4与1mol H2O在2L的密闭容器中反应,6分钟达到平衡,此时CH4的转化率为80%,求这6分钟H2的平均反应速率和该温度下反应的平衡常数是多少?(写出计算过程,结果保留小数点后一位数字。)
自来水厂的水源水(原水)通常含有各种杂质,必须经过去除固体杂质和悬浮物、消毒、去除异味等一系列净化工序(即净化过程),才能达到使用标准。
(1)原水净化有下列措施:① 过滤,② 添加混凝剂,③ 加入活性炭,④ 加入消毒剂。你认为正确的顺序是;
| A.①②③④ | B.②①③④ | C.②③①④ | D.④①②③ |
(2)原水中可以加入明矾作为混凝剂,从而达到去除固体杂质和悬浮物,其原理是明矾溶于水后生成的胶体可以吸附水中的悬浮颗粒并使之沉降。写出明矾中的Al3+水解生成胶体的离子方程式_________________________________________________;
(3)目前我国不少自来水厂采用液氯消毒,液氯注入水中与水发生可逆反应,生成一种强酸和一种弱酸(次氯酸),该反应的化学方程式为______________________________。
按要求回答下列问题
(1)高温和紫外线都可以杀菌消毒,其原因是;
(2)碳酸氢钠是一种常见的疏松剂,在加热条件下产生气体,使食品变的疏松的原理是(用化学方程式表示)。
用中和滴定法测定烧碱的纯度,若烧碱中含有少量不与酸作用的可溶性杂质,试根据实验回答:
(1)准确称取4.1g烧碱样品。
(2)将样品配成250mL待测液,需要的仪器有小烧杯、玻璃棒、、胶头滴管。
(3)用量取10mL待测液于中(填仪器名称),并滴加几滴甲基橙作指示剂。
(4)用0.2010 mol·L-1标准盐酸滴定待测烧碱溶液,滴定时手旋转式滴定管的玻璃活塞,手不停地摇动锥形瓶,两眼注视锥形瓶内溶液颜色的变化,直到滴定终点,滴定终点时锥形瓶内溶液的PH约为,达到终点的具体现象是:。
(5)若两次实验滴定的数据如下表:
| 滴定次数 |
待测液体积(mL) |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
10.00 |
0.50 |
20.4 |
| 第二次 |
10.00 |
4.00 |
24.1 |
据上表数据,计算待测烧碱溶液的浓度:。
(6)根据上述各数据,计算烧碱的纯度:
(7)滴定时,滴定管尖嘴部分滴定前有气泡,滴定终了无气泡,测定结果将_______(填偏高、偏低或无影响,其它操作均正确)。
废电池为什么不能随意丢弃?正确的处理方式是什么?
下面是两位同学关于吸热反应和放热反应的对话,你同意哪位同学的说法?请陈述理由。
甲同学:凡经加热而发生的化学反应都是吸热反应。
乙同学:不一定。有些反应在启动时要加热,反应开始后不再加热就能继续进行,如燃烧反应,这类反应属于放热反应。