将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应:H2(g)+Br2(g)  2HBr(g)
2HBr(g)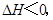 平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是
平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是
| A.a>b | B.a="b" | C.a<b | D.无法确定 |
脑白金可以调整人体生物节律,达到改善睡眠的作用,是一种良好的保健品。脑白金主要成分的结构简式如右图所示,下列对脑白金主要成分的推论正确的是:()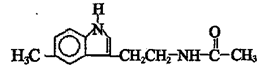
| A.该物质有苯环属于芳香烃,1mol该物质能与5molH2加成 |
| B.其分子式为C13H15N2O |
| C.该物质不能与溴水反应 |
| D.该物质能发生水解反应并生成乙酸 |
下列溶液中各微粒的浓度关系正确的是:()
A.10 ml 0.3 mol/L 的NaCl 溶液与30 ml 0.l mol/L的AlCl3溶液中,Cl—浓度比为1:3
B.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:
c(Na+)>c(HX)>c(X-)>c(H+)>(OH-)
C. 0.1 mol / L的NaHA溶液,其pH = 4:c (HA-) > c (H+) > c (H2A) > c (A2-)
D. pH=3的Na2SO4和盐酸的混合溶液中:c(Na+)=2c(SO42-)
下列实验方案正确且能达到相应实验预期目的的是( )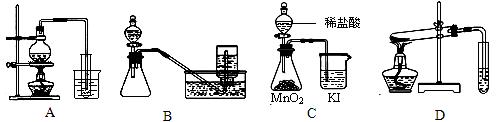
| A.制取少量蒸馏水 | B.用铜和浓硝酸制取少量NO2 |
| C.比较MnO2、Cl2、I2的氧化性 | D.探究NaHCO3 的热稳定性 的热稳定性 |
以下为在浓盐酸中H3AsO3与SnCl2反应的离子方程式,关于该反应的说法正确的组合是:( )
a SnCl2+b Cl-+c H3AsO3+d H+=e As+f SnCl62-+g M
①氧化剂是H3AsO3;②M为OH-;
③每生成7.5gAs,还原剂失去的电子为0.3mol;④ SnCl62-是氧化产物。
| A.①③④ | B.①②④ | C.①②③④ | D.只有①③ |
观察图示装置,下列说法错误的是:()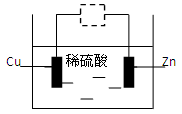
| A.虚线框内接灵敏电流计,该装置可将化学能转化为电能 |
B.虚线框中接直流电源,可能发生反应:Cu + H2SO4  CuSO4 + H2↑ CuSO4 + H2↑ |
C.虚线框内接直流电源,可能发生反应:Zn + H2SO4  ZnSO4 + H2↑ ZnSO4 + H2↑ |
| D.生成2.24 LH2时,一定转移0.2 mol电子 |