今有一混合物的水溶液,可能大量含有以下离子中的若干种:K+、NH4+、Cl—、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验,以下针对原溶液的推测正确的是
| A.Cl—一定不存在 | B.K+一定存在 |
| C.Mg2+一定存在 | D.Ba2+可能存在 |
设nA为阿伏加德罗常数的数值, 下列说法正确的是
下列说法正确的是
| A. 30gC2H6中含有6nA个C-H键 | B.1mol·L-1NaCl溶液中含有nA个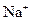 |
| C. 1mol Cu和足量稀硝酸反应产生nA个NO分子 | |
| D.常温常压下,22.4L CO2中含有nA个CO2分子 |
下列叙述正确的是
A.Li在氧气中燃烧主要生成Li2O2
B.将SO2通入BaCl2溶液可生成BaSO3沉淀
C .将CO2通入次氯酸钙溶液可生成次氯酸
.将CO2通入次氯酸钙溶液可生成次氯酸
D.将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu
下列关于电解质溶液的正确判断是
A.在pH = 12的溶液中,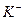 、 、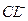 、 、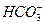 、 、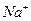 可以大量共存 可以大量共存 |
|
B.在pH= 0的溶液中,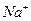 、 、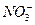 、 、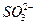 、 、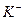 可以大量共存 可以大量共存 |
|
C.由0.1 mol·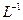 一元碱BOH溶液的pH=10,可推知BOH强碱 一元碱BOH溶液的pH=10,可推知BOH强碱 |
D.由0.1 mol·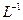 一元酸HA溶液的pH=3, 可推知NaA溶液呈碱性 一元酸HA溶液的pH=3, 可推知NaA溶液呈碱性 |
电解100mL含c(H+)=0.30mol/L的下列溶液,当电路中通过0.04mol电子时,理论上析出金属质量最大的是
| A.0.10mol/LAg+ | B.0.02mol/L Zn2+ |
| C.0.20mol/L Cu2+ | D.0.20mol/L Pb2+ |
下列指定微粒的个数比为1︰2的是
A Be2+离子中的质子和电子 B氘原子中的中子和质子
C NaHCO3晶体中的阳离子和阴离子 D Na2O2固体中的阴离子和阳离子