在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是
A.CH3OH(l)+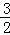 O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ/mol O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ/mol |
| B.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=﹣1452kJ/mol |
| C.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=﹣725.8kJ/mol |
| D.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=+1452kJ/mol |
25℃时,溶液均为0.2 mol•L-1的Na2CO3和NaHCO3溶液中,下列判断不正确的是
| A.均存在电离平衡和水解平衡 |
| B.存在的粒子种类相同 |
| C.c(OH-)前者大于后者 |
| D.分别加入NaOH固体,恢复到原温度,c(CO32-)均增大 |
对pH值相同的盐酸和醋酸两种溶液的说法正确的是
| A.中和碱的能力相同 | B.盐酸和醋酸的物质的量浓度相同 |
| C.OH-的物质的量浓度相同 | D.H+的物质的量浓度不同 |
下列离子方程式中,属于水解反应的是
A.HCOOH+H2O HCOO-+H3O+ HCOO-+H3O+ |
B.CO2+H2O HCO3-+H+ HCO3-+H+ |
C.CO32-+H2O HCO3-+OH- HCO3-+OH- |
D.HS-+H2O S2-+H3O+ S2-+H3O+ |
关于溶液的酸碱性说法正确的是
| A.c(H+)很小的溶液一定呈碱性 | B.pH=7的溶液一定呈中性 |
| C.c(OH-)=c(H+)的溶液一定呈中性 | D.能使酚酞试液变红的溶液一定呈酸性 |
常温下向10mLpH=3的醋酸溶液中加入水稀释后,下列说法正确的是
| A.溶液中导电粒子的数目增加,导电性增强 |
| B.醋酸的电离程度增大,[H+]减小 |
| C.再加入10mL pH="11" NaOH溶液,混合液pH=7 |
| D.溶液中由水电离出的[H+]=1×10-11mol•L-1 |