硫及其化合物在工业生产中有重要的应用,它们性质的研究对工业生产有重要的指导意义。
(1)2SO2(g)+O2(g) 2SO3(g),反应过程的能量变化如图所示。
2SO3(g),反应过程的能量变化如图所示。
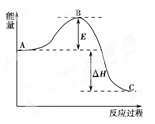
已知1 mol SO2(g)氧化为1 mol SO3(g)放出的热量为99 kJ。请回答下列问题:
①图中E表示_____________,E的大小对该反应的反应热有无影响?_______________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?____________,理由是_____________;
②图中ΔH=____________kJ·mol-1;
(2)下图表示在密闭容器中反应2SO2+O2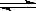 2SO3 达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况。
2SO3 达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况。
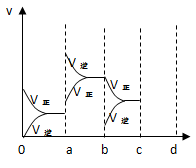
①a b过程中改变的条件可能是 ;
②b c过程中改变的条件可能是 ;
③若增大压强时,反应速率变化情况画在c~d处。
从樟科植物枝叶提取的精油中含有下列甲、乙两种成分: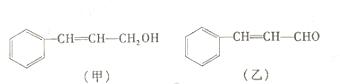
(1)甲中含氧官能团的名称为,乙中含氧官能团的名称为。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):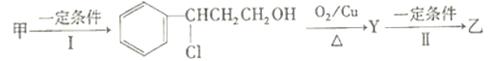
其中反应Ⅰ的反应类型为,反应Ⅱ的化学方程式为:
(注明反应条件)。
(1)在一定条件下制备氯乙烷(C2H5Cl),试回答:
①用乙烷制备氯乙烷的化学方程式是,
该反应的类型是。
②用乙烯制备氯乙烷的化学方程式是,
该反应的类型是。
比较上述两种方法,第种(填“①”或“②”)方法更好。
(2)聚乙烯塑料是由石油裂解产物乙烯通过加聚反应制得,写出乙烯反应生成聚乙烯的化学方程式。
该反应的类型是。
有A、B、C、D、E五种元素,它们可能是原子或离子,且均为短周期元素,A与B可形成BA型化合物,且A是非金属性最强的元素。金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8个;C元素有三种同位素C1、C2、C3,自然界里含量最多的是C1,C3原子的质量数是C1的3倍,C2原子的质量数是C1的2倍。D的气态氢化物水溶液显碱性,而其最高价氧化物水化物为强酸。E元素原子的最外层电子数比次外层电子数多4个,E离子的核外电子数比质子数多2个。
(1)写出A元素名称:___________;
C2粒子的符号:___________;
画出E离子的结构示意图:______________;
A与C形成的化合物所含的化学键类型是:___________。
(2)写出D单质与E单质化合反应的化学方程式:_____________________。
(3)写出B的单质与水反应的溶液混合后发生的反应的离子方程式:
_______________。
(12分)下表是元素周期表的一部分,针对表中的①~⑧元素,填写下列空白:
| ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
||
| 2 |
① |
② |
||||||
| 3 |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
(1)①的气态氢化物分子的空间构型为__________________。
(2)②的气态氢化物稳定性比⑦的气态氢化物_________(填“强”、“弱”或“相同”)。
(3)由①与②形成的三原子分子的电子式为______________________。
由③与⑧形成的离子化合物的电子式为______________________。
(4)③、④、⑤离子半径依次___________。(填“增大”、“减小”或“不变”)
(5)⑤的最高价氧化物对应水化物与③的最高价氧化物对应水化物反应离子方程式为:
。
在一定条件下,可逆反应:a A+b B  cC达到平衡,若:
cC达到平衡,若:
(1)A、B、C都是气体,减少压强,平衡向正反应方向移动,则a+b和c的关系是 。
(2)A、C是气体,增加B的量,平衡不移动,则B为 态。
(3)A、C是气体,而且a+b=c,增大压强可使平衡发生移动,则平衡移动的方向是 。
(4)加热后,可使C的质量增加,则正反应是 反应(填“放热”或“吸热”)。