常温下,取0.3 mol/L HY溶液与0.3 mol/L NaOH溶液等体积混合(不计混合后溶液体积变化),测得混合溶液的pH=9,则下列说法(或关系式)正确的是
| A.混合溶液中由水电离出来的c(OH-)=1×10-9 mol/L |
| B.混合溶液中离子浓度大小次序为:c(Y-)>c(Na+)>c(OH-)>c(H+) |
| C.c(OH-)-c(HY)=c(H+)=1×10-9 mol/L |
| D.c(Na+)=c(Y-)+c(HY)="0.3" mol/L |
某晶体的一部分如下图所示,这种晶体中A、B、C三种粒子数之比是( )
A.3∶9∶4B.1∶4∶2 C.2∶9∶4D.3∶8∶4
下图为冰的一种骨架形式,依此为单位向空间延伸,请问该冰中的每个水分子有几个氢键( )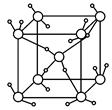
| A.2 | B.4 | C.8 | D.12 |
金刚石是由碳原子所形成的正四面体结构向空间无限延伸而得到的具有空间网状结构的原子晶体。在立方体中,若一碳原子位于立方体中心,则与它直接相邻的四个碳原子位于该立方体互不相邻的四个顶点上(如下图中的小立方体)。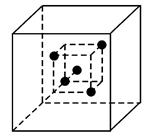
请问,图中与小立方体顶点的四个碳原子直接相邻的碳原子数为多少,它们分别位于大立方体的什么位置( )
| A.12,大立方体的12条棱的中点 |
| B.8,大立方体的8个顶点 |
| C.6,大立方体的6个面的中心 |
| D.14,大立方体的8个顶点和6个面的中心 |
如下图,在氯化钠晶体中,与每个Na+等距离且最近的几个Cl-所围成的空间几何构型为( )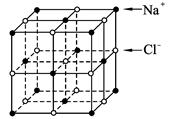
| A.十二面体 | B.正八面体 | C.正六面体 | D.正四面体 |
X、Y是短周期元素,它们可组成化合物XY,则下列说法正确的是( )
| A.XY晶体一定是离子晶体 |
| B.若Y的原子序数为m,X的原子序数一定是m±6 |
| C.X、Y可以属于同一周期,也可属于两个不同周期 |
| D.X与Y一定不属于同一主族 |