已知一定条件下断裂1 mol下列化学键生成气态原子需要吸收的能量如下:H—H 436 kJ;Cl—Cl 243 kJ;H—Cl 431 kJ。下列所得热化学方程式或结论正确的是
| A.H(g) + Cl(g) =HCl(g) ΔH=﹣431 kJ·mol-1 |
| B.2HCl(g) = H2(g) + Cl2(g)的反应热ΔH<0 |
| C.H2(g) + Cl2(g) = 2HCl(g) ΔH=﹣183 kJ |
| D.相同条件下,H2(g)+ Cl2(g) =2HCl(g)反应在光照和点燃条件下的ΔH不相等 |
(07年广东卷)下列说法中正确的是
A石油裂解可以得到氯乙烯 B油脂水解可得到氨基酸和甘油
C所有烷烃和蛋白质中都存在碳碳单键 D淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖
有关糖类物质概念的叙述中,正确的是()
| A.糖类是有甜味的物质 | B.糖类是具有CN(H20)m通式的物质 |
| C.糖类是含有醛基或羟基的物质 | D.糖类一般是多羟基醛或多羟基酮以及能水解生成它们的物质 |
酶是蛋白质,因而具有蛋白质的特性,酶又是生物制造出来的催化剂,能在许多有机反应中发挥作用,以下表示温度t与反应速度v的关系曲线中,有酶参加的是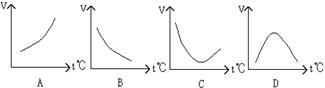
化学反应C(s)+H2O(g) 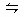 CO(g)+H2(g) ΔH>0达到平衡,下列叙述中正确的是 ( )
CO(g)+H2(g) ΔH>0达到平衡,下列叙述中正确的是 ( )
| A.升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
| B.加入固体碳,平衡向正反应方向移动 |
| C.加入水蒸气使容器内压强增大,平衡向逆反应方向移动 |
| D.扩大容器容积,平衡向正反应方向移动 |
对于反应2A(g)+B(g) 2C(g)△H<0,下列图象正确的是()
2C(g)△H<0,下列图象正确的是()