糕点(如月饼)包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
| A.脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B.脱氧过程中铁作原电池正极,电极反应为:Fe—3e— =Fe3+ |
| C.脱氧过程中碳做原电池负极,电极反应为:2H2O + O2 + 4e—= 4OH— |
| D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) |
成语“恶狗酒酸”中隐藏着一个寓言故事:人有市酒而甚美者,然至酒酸而不售,问里人其故。里人曰:公之狗甚狂,人有持器往者,狗辄迎面啮之,是以酒酸不售也。 下列关于“酒”的说法错误的是
| A.“恶狗酒酸”的成语中涉及了氧化反应 |
| B.糖类、油脂都可以用来酿酒 |
| C.葡萄糖转变成酒精的过程放出热量 |
| D.工业酒精中因含有剧毒物质甲醇而不能用来勾兑饮用酒水 |
下列溶液或浊液中,关于离子浓度的说法正确的是
A.一定浓度的氨水加水稀释的过程中,c(NH4+)/ c(NH3·H2O)的比值减小
B.浓度均为0.1 mol·L-1的Na2CO3、NaHCO3混合溶液中:
c(CO32-) > c(HCO3-),且2c(Na+)=3c(H2CO3)+3c(HCO3-)+3c(CO32-)
C.常温下0.4mol/LHB溶液和0.2mol/LNaOH溶液等体积混合后溶液的pH=3,则溶液中微粒浓度存在下面关系: c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-)
D.假设HClO的电离平衡常数为Ka,碳酸的电离常数分别记为:Ka1和Ka2,已知:Ka1 > Ka > Ka2 , 则发生反应:2NaClO + CO2(少量)+H2O=Na2CO3+2HClO
常温下,向某浓度H2A溶液中逐滴加入一定量浓度NaOH溶液,所得溶液中H2A、HA﹣、A2﹣三种微粒的物质的量分数与溶液pH的关系如图所示,则下列说法中不正确的是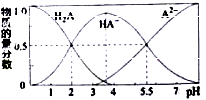
A.H2A是一种二元弱酸
B.常温下,H2A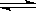 H++HA﹣的电离平衡常数Ka1=0.01
H++HA﹣的电离平衡常数Ka1=0.01
C.将相同物质的量的NaHA和Na2A固体溶于水所得混合溶液pH一定为5.5
D.在量热计中,用20.0mL0.10mol/LNaOH溶液,分别与10.0mL0.20mol/LH2A和20.0mL0.10mol/LH2A反应后放出的热量不相同
室温时,向20 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生,且混合溶液的体积可看成混合前两溶液的体积之和),下列说法不正确的是: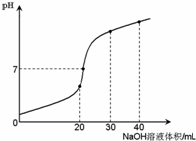
| A.pH=7时,溶液中c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| B.当V(NaOH)=20mL时,溶液中水的电离程度比纯水大 |
| C.当V(NaOH)=30mL时,溶液中 c(SO42-)+ c(H+)= c(NH3·H2O) + c(OH-) |
| D.滴加NaOH溶液从30mL至40mL,溶液中Na+与SO42-浓度之和始终为0.1 mol·L-1 |
下列各组离子在指定溶液中一定能大量共存的是
①pH = 0的溶液:Na+、C2O42—、MnO4—、SO42—
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32-
③水电离的H+浓度为10-12mol·L-1的溶液中:Cl-、CO32-、NO3-、NH4+、SO32-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-
⑤使石蕊变红的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42-
⑥中性溶液中:Fe3+、Al3+、NO3-、I-、Cl-、S2-
| A.①②⑤ | B.①③⑥ | C.②④ | D.①②④ |