通过化学学习,相信你已经初步掌握了实验室制取氧气的有关知识。下列为实验室常用的实验装置,回答有关问题:

A B C D E F G
(1)写出标号仪器名称:① ;② 。
(2)用高锰酸钾固体制氧气,应选用发生装置 (填“A”或“B”),反应的文字表达式是 。
若用过氧化氢溶液和二氧化锰制取氧气,能否选用C 装置 (填“能”或“不能”), 反应的文字表达式是 。你认为上述两种实验室制取氧气的方法中 更好,原因是 。
(3)若要收集较干燥的氧气,应选用收集装置 (填“D”或“E” 或“F”)。
(4)医院给病人输氧时用到装置G,瓶中盛放蒸馏水。以下说法正确的是 (填字母)。
a.导管③连接供给氧气的钢瓶
b.导管③连接病人吸氧气的塑胶管
c.该装置可用来观察输出氧气的速度
(5)实验室用高锰酸钾制取氧气大致可分为以下几个步骤:
①点燃酒精灯,加热试管;
②检查装置的气密性;
③将高锰酸钾装入试管,管口放一小团棉花,塞上带导管的单孔塞;固定在铁架台上;
④用排水法收集氧气;
⑤熄灭酒精灯;
⑥将导气管从水中取出.
正确的操作顺序是 (填字母)。
| A.②③①④⑤⑥ | B.③②①④⑥⑤ |
| C.②③①④⑥⑤ | D.③④①②⑤⑥ |
(6)用排水法收集氧气时,开始收集的适宜时刻是 ,表明氧气已集满的现象是 ,集满氧气的集气瓶应取出 (填“正放”或“倒放”)在桌上。
(7)某班同学在完成氧气的制取时,出现了下面一些情况,请你分析原因:
①在加热高锰酸钾时,水槽中出现的气泡很少。
②用排水法收集时,发现水槽里的水呈紫红色。
③实验结束后,发现有水倒流到试管。
甲、乙、丙是初中化学中常见的物质,其转化关系如下图所示: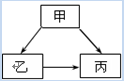
(1)若甲为黑色单质,甲、乙、丙中都含有相同的一种元素。则乙物质是____;甲 丙的化学方程式__ _ _。
丙的化学方程式__ _ _。
(2)若甲物质是氧元素含量最高的氧化物,甲物质与乙物质的组成元素相同,乙常温下呈液态。则乙物质是____;甲 丙的化学方程式_ _ _ _。
丙的化学方程式_ _ _ _。
右下图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据右下图回答下列问题: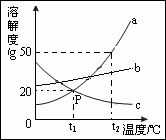
(1)t1℃时15g a物质加入到50g水中不断搅拌,形成的溶液是_ 溶液(填“饱和”或“不饱和”)。
(2)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是(填写物质序号)____ 。
(3)若a中混有少量的b,获得纯净a的方法是__。
被誉为“东方之冠”的中国馆是上海世博会标志性建筑之一,中国馆共向地下钻孔约5000根钢筋水泥桩,其横梁、椽子、斜撑、柱子的“中国红”外衣选用的是铝板,馆周围是大片红木色的塑木(塑料和木屑按照近似于1∶1的比例制成)地板。
(1)下列关于铝合金的说法不正确的是。
| A.具有导电性 | B.银白色 | C.属于单质 | D.属于金属材料 |
(2)铝能与NaOH溶液反应,化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3X↑, X的化学式为。
(3)将铁丝浸入硫酸铜溶液中能形成美丽的“铜树”,发生反应的化学方程式为:
___________,该化学反应的基本类型属于__ _____ 。
用化学符号填空。
(1)磷元素;(2)氯离子;(3)二氧化氮中氮元素的化合价为+4价。
某化学兴趣小组利用下图装置探究制取气体的原理、方法及性质。请结合下图,回答有关问题。
(1)写出图中标号仪器的名称:a,b。
(2)用高锰酸钾制取氧气时,可选用的发生装置是(填写图示字母,下同),可选用C装置收集氧气,其原因是,写出发生反应的化学方程式:。
(3)实验室常选用上述装置作为实验室制取二氧化碳的发生装置,写出实验室制取二氧化碳的化学方程式是;
(4)实验室常用锌和稀硫酸反应制取氢气,反应的化学方程式为___________________,同学们选用上述B装置制取氢气,在将药品加入装置之前,进行的操作为___________,收集氢气可选用的装置是________ 。