设NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.1NA |
| B.电解饱和食盐水,当阴极产生2.24L H2时,转移的电子数为0.2NA |
| C.常温下,1.0L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
| D.将100mL0.1mol·L -1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA |
下列反应的离子方程式正确的是
| A.等物质的量的 Ba (OH )2与 NH4HSO4的稀溶液反应 Ba2+ + 2OH一+2H+ + SO42-=BaSO4↓+2H2O |
| B.向硫酸铜溶液中加入足量的氢氧化钡溶液 Ba2+十SO42-=BaSO4↓ |
| C.向碳酸氢钠洛液中滴入过量石灰水 HCO3-+Ca2+十OH-=CaCO3↓+H2O |
| D.向氯化铝溶液中加入过量的氨水 A13++ 4NH3·H2O=Al(OH)3↓+4NH4+ +2H2O |
对三硫化四磷分子的结构研究表明,该分子中没有不饱和键,且各原子的最外层均已达到了 8 个电子的结构。则一个三硫化四磷分子中含有的共价键个数是
| A.7 个 | B.9 个 | C.19 个 | D.不能确定 |
2008 年北京奥运会主体育场的外形好似“鸟巢” ( The Bird Nest )。有一类硼烷也好似鸟巢,故称为巢式硼烷。巢式硼烷除 B10H14不与水反应外,其余均易与水反应生成氢气和硼酸,硼烷易被氧化。下图是三种巢式硼烷,有关说法正确的是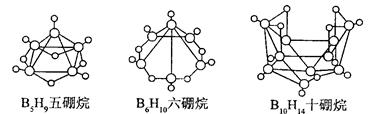
| A.这类巢式硼烷的通式是 C nH n + 4 |
B.2B5H9 + 12O2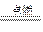 5B2O3 十9H2O ,l molB5H9完全燃烧转移25mol电子 5B2O3 十9H2O ,l molB5H9完全燃烧转移25mol电子 |
| C.8 个硼原子的巢式棚烷化学式应为 B8H10 |
| D.硼烷与水反应是非氧化还原反应 |
下列化学用语正确的是
| A.NH4十电子式:NH4十 |
| B.乙炔的分子式: CH≡CH |
| C.硬脂酸的结构简式: C17H35COOH |
| D.电解时铁作阳极的电极反应式:Fe一3e一= Fe3+ |
英国研究人员 2007 年 8 月 30 日发表报告认为,全球将有 1.4 亿人因为用水而受到砷中毒之害、导致更多的人患癌症。海带含砷超标,经水浸泡 24 小时后,其含砷量才能达到食用安全标准。下列对砷 ( As )的有关判断正确的是
| A.砷原子序数为 33 ,它与铝为同主族 |
| B.砷的原子半径小于磷的原子半径 |
| C.砷化氢的稳定性比溴化氢的强 |
| D.砷酸的酸性比硫酸的弱 |