HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+.AgNO2是一种难溶于水、易溶于酸的化合物.试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+.若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为 Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是____________(填序号)。
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是____________(填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI-淀粉溶液来区别
D. 用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:____________________。
(4)Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是___________(填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2:1,试配平下列方程式:
FeSO4+ K2O2→ K2FeO4+ K2O+ K2SO4+ O2↑
(6)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体.高铁酸钾作为水处理剂发挥的作用是______________________。
在120 ℃时分别进行如下四个反应:
| A.2H2S+O2====2H2O+2S↓ | B.2H2S+3O2====2H2O+2SO2 |
| C.C2H4+3O2=====2H2O+2CO2 | D.C4H8+6O2====4H2O+4CO2 |
(1)当反应在容积固定的容器内进行,反应前后气体密度(d)的气体总压强(p)分别符合关系式d前=d后和p前>p后的是____________;符合关系式d前=d后和p前=p后的是__________。(请填写反应的代号)
(2)若反应在压强恒定容积可变的容器内进行,反应前后气体密度(d)和气体体积(V)分别符合关系式d前>d后和V前<V后的是________,符合d前>d后和V前>V后的是_______。(请填写反应的代号)
如图:在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧分别进行如图所示的可逆反应。各物质的起始加入量如下:A、B和C均为4.0 mol,D为6.5 mol,F为2.0 mol,设E为x mol。当x在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于正中位置。请填写以下空白: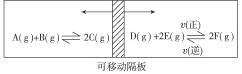
若x=4.5,则右侧反应在起始时向____________(填“正反应”或“逆反应”)方向进行。欲使起始反应维持向该方向进行,则x的最大取值应小于______________。
(2)若x分别为4.5和5.0,则在这两种情况下,当反应达平衡时,A的物质的量_________(填“相等”“不相等”或“不能确定”)。其理由是_______________。
下图所示是可逆反应A+2B 2C+3D的化学反应速率和化学平衡随外界条件改变而变化的情况:
2C+3D的化学反应速率和化学平衡随外界条件改变而变化的情况: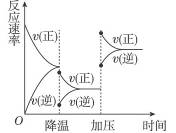
由图可判断:
(1)正反应是_____________(吸热、放热)反应。
(2)若A、B是气体,则C的状态是__________,D的状态是______________。
钾是一种活泼的金属,工业上通常用金属钠和氯化钾在高温下反应制取。该反应为:
Na(l)+KCl(l) NaCl(l)+K(g)-Q
NaCl(l)+K(g)-Q
各物质的沸点与压强的关系如下表。
| 压强/kPa |
13.33 |
53.32 |
101.3 |
| K的沸点/℃ |
590 |
710 |
770 |
| Na的沸点/℃ |
700 |
830 |
890 |
| KCl的沸点/℃ |
1 437 |
||
| NaCl的沸点/℃ |
1 465 |
(1)在常压下金属钾转变为气态从反应混合物中分离的最低温度约为__________,而反应的最高温度应低于__________。
(2)在制取钾的过程中,为了提高原料的转化率可以采取的措施是______________。
已知4℃时四种化合物在水中和液氨中的溶解度如下表:
| AgNO3 |
Ba (NO3)2 |
AgCl |
BaCl2 |
|
| H2O(l) |
170g |
9.20g |
1.50×10-4g |
33.3g |
| NH3(l) |
86.0g |
97.2g |
0.80g |
0.00g |
①上述四种物质能在水中发生的复分解反应为___________________________;
②能在液氨中发生的复分解反应为_____________________________________。