2g Cu2S和CuS的混合物在酸性溶液中用400mL 0.075mol/L KMnO4溶液处理,发生反应如下:
①______MnO4-+______Cu2S+______H+=______Cu2++______SO2+______Mn2++______H2O
②6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液赶尽SO2,剩余的KMnO4恰好与350mL0.1mol/L(NH4)2Fe(SO4)2溶液完全反应,反应式为:③MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
请回答:
(1)配平KMnO4与Cu2S反应的离子方程式:
______MnO4-+______Cu2S+______H+=______Cu2++______SO2+______Mn2++______H2O,若标准状况下有1.12L SO2生成,则被还原的MnO4—物质的量是 。
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为__________mol。
(3)混合物中Cu2S的质量分数为__________。
已知碳碳双键可以被臭氧氧化:
有机物A可以发生如下图所示的变化,其中E不能发生银镜反应,M的分子内含有七元环状结构。
(1)A的结构简式为________。
(2)A~M中,互为同系物的是________(填字母代号)。
(3)B的同分异构体中,具有链状结构的酯类物质有________种,请写出其中一种物质的结构简式:________。
(4)写出下列反应的化学方程式。
①F―→G:______________________。
②C+L―→M:______________________。
(1)饱和一元醇通式为CnH2n+1OH。
①出现醇类同分异构体时,n最小值为________;
②出现官能团异构体时,n最小值为________。
(2)已知戊醇(C5H12O)共有8种属于醇类的异构体,请回答:
①在戊醇的这些同分异构体中,能氧化生成醛的有4种,它们的结构简式分别是________、________、________、________。
②这8种同分异构体脱水后可得________种烯烃。
2009年甲型H1N1流感横行墨西哥,进而扩散全球,莽草酸是合成治疗甲型H1N1流感的药物——达菲(Tamiflu)的原料之一。莽草酸是A的一种同分异构体。A的结构简式如下: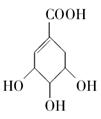
(1)A的分子式是________。
(2)A与溴的四氯化碳溶液反应的化学方程式(有机物用结构简式表示)是________。
(3)A与氢氧化钠溶液反应的化学方程式(有机物用结构简式表示)是_____。
(4)A在浓硫酸作用下加热可得到B(B的结构简式为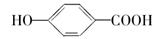 ,其反应类型是________。
,其反应类型是________。
(5)B的同分异构体中既含有酚羟基又含有酯基的共有________种,写出其中一种同分异构体的结构简式:______________________________。
X、Y、Z、W是短周期的四种元素,有关他们的信息如表所示。
| 元素 |
部分结构知识 |
部分性质 |
| X |
X的单质由双原子分子构成,分子中有14个电子 |
X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y |
Y原子的次外层电子数等于最外层电子数的一半 |
Y能形成多种气态氢化物 |
| Z |
Z原子的最外层电子数多于4 |
Z元素的最高正化合价与最低负化合价代数和等于6 |
| W |
W原子的最外层电子数等于2n-3(n为原子核外电子层数) |
化学反应中W原子易失去最外层电子形成Wn+ |
填写下列空白(不能用字母X、Y、Z、W作答)。
(1)X的气态氢化物分子的电子式是,Z元素在周期表中的位置是。
(2)X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是。
(3)常温时,W的硫酸盐溶液的pH(填“>”、“<”或“=”)7,理由是:(用离子方程式表示)。
(4)实验室用X的氢化物的水溶液制取W的氢氧化物的方法是(用离子方程式表示)。
(5)25℃、101 kPa时,32 g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6kJ的热量,写出该反应的热化学方程式:。
短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物。
请回答:
(1)X的原子结构示意图是;Y的元素符号是;Z元素的名称是。
(2)XZ3化合物的电子式是。
(3)X的最高价氧化物的分子式是;Y的最高价含氧酸的结构简式是。