某同学在用稀盐酸与铁制取氢气的实验中,发现加入少量氯化铜溶液可加快氢气的生成速率。请回答下列问题:
(1)要加快上述实验中气体产生的速率,还可采取的措施有
(答两种);
(2)实验室中现有NaCl、CuSO4、FeCl2、ZnCl2等4种溶液,可与实验中CuCl2溶液起相似作用的是 ;
(3)为了进一步研究氯化铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验(混合溶液) |
A |
B |
C |
D |
E |
F |
| 4mol/L 盐酸/mL |
60 |
V1 |
V2 |
V3 |
V4 |
V5 |
| 饱和CuCl2溶液/mL |
0 |
1.0 |
5.0 |
10 |
V6 |
40 |
| H2O/mL |
V7 |
V8 |
V9 |
V10 |
20 |
0 |
①请完成此实验设计,其中:V1= ,V6= ,V9= ;
②该同学最后得出的结论为:当加入少量CuCl2溶液时,生成氢气的速率会
大大提高。但当加入的CuCl2溶液超过一定量时,生成氢气的速率反而会下降。
请分析氢气生成速率下降的主要原因
氯化铍是用于制有机铍化合物和金属铍的重要原料。
(1)BeCl2分子中组成元素Be的基态原子的价电子排布式为,其元素的第一电离能B元素(填“>”或“<” 或“=”),原因是。
(2)已知BeCl2加热易升华,液态BeCl2不导电,BeCl2晶体类型为; BeCl2中Be原子的杂化轨道类型是。
(3)用阴离子树脂交换法提取一种组成元素为氯和铍的阴离子,该阴离子内铍原子达到8电子稳定结构,则该离子内存在的微粒间的作用力是,阴离子的结构式为。
、钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”。试回答下列问题:
(1)钛有 Ti和
Ti和 Ti两种原子,它们互称为。Ti元素在元素周期表中的位置是第周期,第族;按电子排布Ti元素在元素周期表分区中属于(填s、p、d、ds或f)区元素
Ti两种原子,它们互称为。Ti元素在元素周期表中的位置是第周期,第族;按电子排布Ti元素在元素周期表分区中属于(填s、p、d、ds或f)区元素
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用。偏钛酸钡为离子晶体,晶胞的结构如右图所示,它的化学式是
(3)现有含Ti3+的配合物,化学式为TiCl3(H2O)6,将1mol该物质溶于水,加入足量硝酸银溶液,立即沉淀的氯化银为1mol,已知该配合物的配位数为6,则该配合物的配位体是。
1mol该配合物外界所含结晶水物质的量为mol。
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为。
(2)B的氢化物的分子空间构型是。其中心原子采取杂化。
(3)写出化合物AC2的电子式;一种由B、C组成的化合物与AC2互为等电子体,其化学式为。
(4)ECl3与B、C的氢化物形成配位数为六的配合物的化学式为。
短周期元素X、Y、Z在周期表中位置关系如图:(答题时,X、Y、Z用所对应的元素符号表示)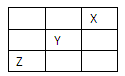
(1)x元素的单质分子式是_______,单质是_______晶体。
(2)自然界中存在一种仅含钙与Y两种元素的天然矿物,其电子式为_______,属于_______晶体。
(3)Z的氢化物和Y的氢化物沸点高低顺序是:,理由:
。
(4)X、Y、Z三种元素中,电负性最大的是:。
(1)具有支链的化合物A的分子式为C4H6O2,A可以使Br2的四氯化碳溶液褪色。1molA和1mol NaHCO3能完全反应,则A的结构简式是,写出与A具有相同官能团的A的所有同分异构体的结构简式
(2)化合物B含有C、H、O三种元素,分子量为60,其中碳的质量分数为60%,氢的质量分数为13.33%。B在催化剂Cu的作用下被氧化成C,C能发生银镜反应,则B的结构简式是
⑶某有机物完全燃烧,生成标准状况下CO2的体积为4.48 L,H2O的质量为5.4g。
①若有机物的质量为4.6g,此有机物的分子式为
②若有机物的质量为6.2g,且此有机物lmol能和足量的金属钠反应生成lmolH2,此有机物的结构简式为(两个羟基不能连在同一个碳原子上)