已知反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,若有2.24LCl2(已换算为标准状况)生成,请回答:
(1)HC1在该反应过程中表现出的化学性质有___________。
| A.酸性 | B.还原性 | C.氧化性 | D.挥发性 |
被氧化的HCl为____________g,转移电子数目为_________________。
(2)用“双线桥”或“单线桥”标出上述反应的电子转移方向和数目
分甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质。
(1)一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH1
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)ΔH2
现有一份在相同条件下对H2的相对密度为17的NO与NO2的混合气体,用16 g甲烷气体催化还原该混合气体,恰好生成氮气、二氧化碳气体和水蒸气,共放出1042.8 kJ热量。
①该混合气体中NO和NO2的物质的量之比为____________。
②已知上述热化学方程式中ΔH1=-1160 kJ/mol,则ΔH2=____________。
③在一定条件下NO气体可以分解为NO2气体和N2气体,写出该反应的热化学方程式:______________。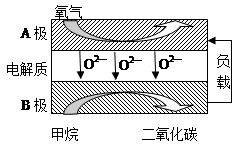
(2)以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛地研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
④B极为电池____________极,电极反应式为________________。
⑤若用该燃料电池作电源,用石墨作电极电解100 mL 1 mol/L的硫酸铜溶液,当两极收集到的气体体积相等时,理论上消耗的甲烷的体积为______________(标准状况下),实际上消耗的甲烷体积(折算到标准状况)比理论上大,可能原因为________________。
某温度时,在2L容器中X、Y、Z三种物质的物质的量随时间的变化关系曲线如图所示。
(1)由图中的数据分析,该反应的化学方程式为 ___________
(2)反应开始至2min、5minZ的平均反应速率为 、 ;
(3)5min后Z的生成速率比5min末Z的生成速率 (填写“大、小或相等”)。
1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH发生中和反应的中和热为_______,表示该中和热的热化学方程式为________
如右图所示装置为在直流电流作用下电解CuSO4溶液图,其中A、B为石墨电极,a、b为电源的两极,当接通电源后,通电一段时间后,将B电极取出洗干净并干燥后称量其质量增加了3.2g,则: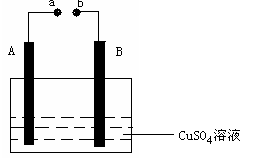
(1)a为电源的 极。B叫电解槽的 极,电路中流过的电子的数目为
(2)写出电极反应方程式:A ,B 。
(3)如果想使反应溶液恢复到原来状态,应该加入 g
家用炒菜铁锅用水清洗放置后,便会因腐蚀而出现红棕色的锈斑,铁锅发生腐蚀应属于 腐蚀,负极反应式为 ,正极反应式为 ,